阻断肌萎缩侧索硬化症中有毒蛋白的产生
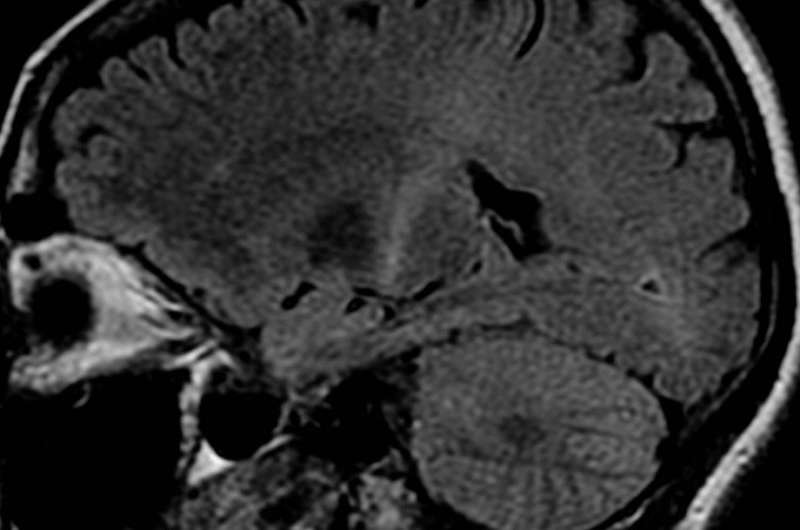
肌萎缩性侧索硬化症患者的大脑细胞中经常有一串重复的DNA密码,C9orf72基因中有数百到数千个副本。一项新的研究研究了是什么触发了这些重复序列,最终产生与肌萎缩性侧索硬化症、额颞叶痴呆和其他神经退行性疾病相关的有毒蛋白质,这些疾病是携带C9orf72突变的患者最常见的遗传性肌萎缩性侧索硬化症的病因。该研究发现,神经元兴奋和应激会触发细胞内蛋白质的产生,并揭示了用已知药物针对这种应激反应可以减少有毒蛋白质的产生。
“了解有毒蛋白质产生的触发器有助于我们磨练可以阻止它们的药物实验室测试Aaron Haeusler博士是Vickie & Jack Farber神经科学研究所和Weinberg肌萎缩侧索硬化症中心(费城大学+托马斯杰弗逊大学)的神经科学助理教授。这项研究发表在EMBO分子医学。
通过与共同首席研究员Davide Trotti博士和共同作者Piera Pasinelli博士(Jefferson Weinberg ALS Center的负责人)的合作,Haeusler博士和他的同事测试了导致C9orf72内重复DNA序列激活和产生的原因有毒蛋白质。怀疑压力因子作为可能的触发,调查人员测试了许多导致神经元转动应力反应的药剂。实际上,许多这些也开始产生有毒蛋白质。研究人员还表明神经元过度激发,类似于在癫痫发作期间发生的事情,也引发了蛋白质生产。
“两个都细胞压力并过度激励最终会聚到集成的应激反应第一作者托马斯韦斯特加德(Thomas Westergard)说。他是特洛蒂博士实验室的研究生。
一旦整合的应激反应被激活,就很难停止这些有毒蛋白质的产生。但是,通过对这种包罗一切的细胞机制的研究,研究人员得以窥见可能阻断神经元损伤反应的具体方法。
已被批准用于治疗抑郁症的药物曲唑酮,已知对综合应激反应的某些部分起作用。因此,研究人员在他们的疾病模型中测试了这种药物,发现它确实可以阻止含有重复突变的细胞模型中有毒蛋白质的产生。
“这是我们的重要一步合作方式“博士博士说,”共同努力允许我们加快识别“致病胁迫”来测试潜在有用的药物的研究进程。ALS是一种复杂和异因疾病,需要这种协作方法,每个实验室都有贡献自己的专业知识,以填补空白并以系统和有效的方式将这种复杂的拼图放在一起,“
研究人员现在正在扩展他们的研究,对其他可能比药物曲氮酮更好的其他分子筛选。












用户评论