实验治疗显示了对抗三阴性乳腺癌的希望
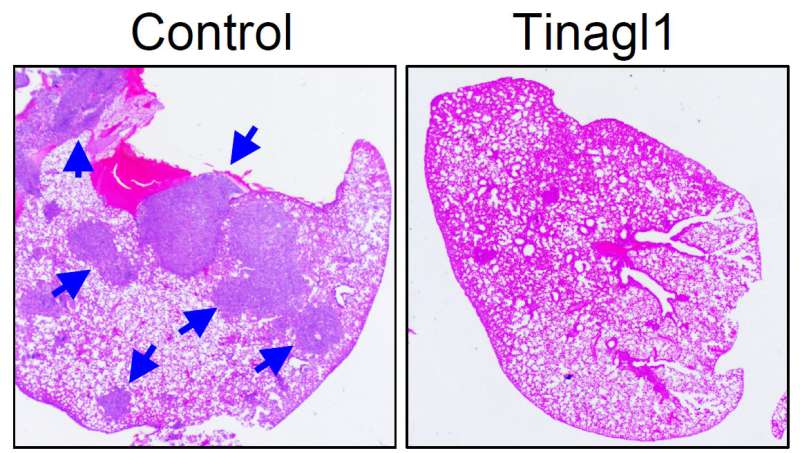
通过同时处理癌症生长的两种机制,一项在小鼠身上进行的实验治疗减少了三阴性乳腺癌的扩散。
这种名为Tinagl1的治疗剂是以一种自然产生的蛋白质为基础的,它可以阻断两种主要途径乳腺癌细胞能否生长和迁移出原发肿瘤扩散到身体的其他器官。该研究发表在该杂志上癌症细胞1月3。
“人们试图阻止这种形式的传播癌症但迄今为止尝试已经失败了,因为如果你尝试的一种方法,癌细胞补偿通过寻找一种逃避,“宜宾Kang说,华纳兰波特/ Parke-Davis普林斯顿大学分子生物学教授,副主任财团新泽西州罗格斯大学癌症研究所研究,这项研究的资深作者。“有了这种新方法,治疗同时阻断了这两种途径。这就像一石二鸟。”
三阴性乳腺癌是一种高度侵袭性的癌症,发病率占所有乳腺癌病例的12%至17%。它的名字来自于缺乏三个突出的生物目标雌激素受体受体(ER)、孕激素受体(PR)和人类表皮生长因子受体2 (HER2)——它们被用来发现和杀死癌细胞。
三阴性乳腺癌患者复发率高且较少治疗方案以及癌症对治疗产生耐药性的可能性。这导致患者的整体预后较差。
新的发现表明,重组的Tinagl1是进一步探索和发展治疗这种癌症的一个很好的候选药物。
研究人员发现,Tinagl1抑制了导致三阴性乳腺癌侵袭性和抵抗治疗能力的两种主要途径。Tinagl1以不同的方式抑制了这两种途径,克服了癌症用来逃避治疗的补偿机制。
Tinagl1通过阻止肿瘤细胞的活动来治疗癌症肿瘤促蛋白,即表皮生长因子受体基因(EGFR)。该基因的突变导致EGFR信号活性激增,向细胞发送促生长信号并加速肿瘤的生长并转移到身体的新部位。针对表皮生长因子受体的治疗方法临床成功有限,可能是因为癌细胞找到了新的生长途径。
这种蛋白质对被称为整合素的分子也有影响,整合素参与调节细胞迁移到新位置、与其他细胞的粘附以及转化为肿瘤。Tinagl1似乎能够通过干扰一种名为focal adhesion kinase (FAK)的相关蛋白来靶向整合素信号,FAK促进细胞迁移、生长和存活。
据研究人员称,这两条途径在分子上是相互关联的,导致了三阴性乳腺癌的侵袭性和耐药性的冗余和补偿。
研究人员观察了800多份取自人类患者的乳腺肿瘤样本。他们发现,Tinagl1基因表达较低的肿瘤样本更有可能来自肿瘤晚期和存活时间较短的患者。该基因水平较高的肿瘤与患者的良好预后有更强的联系。
这种差异在乳腺癌的三阴性亚组中最为显著。
为了测试Tinagl1基因是否可以防止肿瘤生长和扩散,研究人员对人类和小鼠的肿瘤进行了工程设计细胞高水平表达Tinagl1基因。研究人员发现Tinagl1在小鼠体内高表达癌症细胞产生生长较慢的肿瘤,不太可能转移到肺部。
研究人员还给患有乳腺肿瘤的小鼠注射了Tinagl1蛋白,结果发现,7周的治疗显著抑制了原发肿瘤生长和自发性肺转移,而没有明显的副作用。在一项关于Tinagl1发生时间的研究中治疗在美国,这种化合物即使在肿瘤开始转移后仍然有效。该团队还研究了Tinagl1抑制的机制,发现该蛋白同时抑制EGFR和整合素/FAK信号通路,因此比使用单一抑制剂对这两种通路都有更好的效果。
“Tinagl1抑制三阴性乳腺癌通过同时抑制整合素/FAK和EGFR信号,来实现进展和转移。癌症细胞2019年1月3日。











用户评论