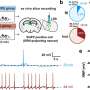
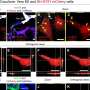
帕金森氏症小鼠大脑活动模式的改变
帕金森氏症的蛛丝马迹来自于大脑中一个对自主运动至关重要的区域的异常活动。冲绳科学技术研究生院(OIST)的研究人员使用这种疾病的小鼠模型,确定了大脑活动的不寻常模式,这似乎是其标志性症状的基础。
帕金森氏症破坏了基底神经节这组核将信息从褶皱的皮层传递到对运动控制很重要的大脑区域。一个被称为纹状体的核作为整个结构的主要输入中枢。标记为急剧下降在化学信使多巴胺和制造多巴胺的细胞中,帕金森症剥夺了基底神经节正常运作所需的工具,并将纹状体推向病理性亢进。
“当你把多巴胺拿走时,细胞重新组织,这种重新组织导致了帕金森氏症的大部分症状,”该研究的高级作者、OIST行为单元大脑机制的首席研究员戈登·阿布特诺特教授说。这项研究于2019年1月30日在网上发表欧洲神经科学杂志,表明纹状体神经元当细胞缺乏多巴胺时,正常的活动模式就会发生变化。这种模式由一个特定的细胞子集主导,通常是同步放电。具有这种大脑活动模式的小鼠在重复的圆圈中转动,这在帕金森症小鼠模型中是典型的。
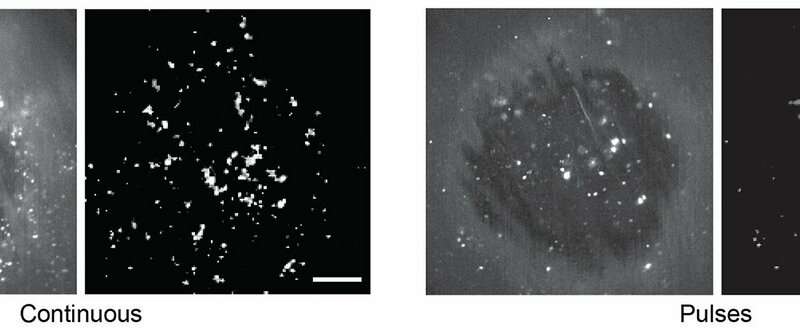
科学家们更进一步:通过将神经元与光敏蛋白质在美国,他们能够通过将正常小鼠暴露在光线下来提高它们的纹状体活动。值得注意的是,神经元对不同模式的光有不同的反应。连续的光线重现了异常的同步模式,并使小鼠向一个方向转动。但脉冲光激发的神经元更少,引发的纹状体活动更典型,实际上导致小鼠转向另一个方向。
“事实是,当我改变刺激时,动物转向相反的方向——这令人震惊,”该研究的第一作者奥马尔·贾达尔博士说,他当时是Arbuthnott单位的博士后学者。(贾达尔现在是斯坦福大学丁俊教授的博士后。)观察结果表明,帕金森综合症的出现是由于许多神经元同步被强烈激活,而不受调节多巴胺信号的影响。
“你需要一定的肌肉序列来收缩来执行任何动作,[纹状体]神经元也是如此,”贾达尔说。纹状体神经元群倾向于按顺序放电,相当均匀地分配它们的工作。他说,如果这种活动模式不能维持,纹状体就不能正常工作。“人们必须更深入地研究神经元放电的序列;这可能对未来的治疗很重要。”
挑战帕金森病的旧模型
这些结果与现有的帕金森病模型相矛盾,现有模型关注的是这种疾病如何影响不同类型的神经元。两种被称为纹状体输出神经元的细胞在纹状体中接受多巴胺并对其信号作出反应。第一种类型被称为D1神经元,被认为有助于发起运动,而D2神经元则抑制运动。正常情况下,这些细胞协同工作,实时调节运动,就像汽车的油门踏板和刹车一样。许多模型表明,D2神经元在帕金森氏症中过度活跃,抑制运动到导致僵硬、颤抖甚至冻结的程度。
但现实可能没有这么简单。
“细胞不仅有‘正’和‘负’,它们还有模拟信号,”Arbuthnott说。“如果你有一大群人,信号就会更加复杂。”新的研究表明D1和D2神经元对帕金森模型中出现的异常大脑活动也有同样的影响。这不是D2压倒D1的问题,而是整个系统在没有的情况下扭曲了多巴胺.
通过了解脑回路水平上的活动模式是如何变化的,科学家们或许能够开发出更好的帕金森氏症干预措施。例如,这一研究方向可能会揭开如何深部脑刺激有助于缓解帕金森症状有更好的电刺激方法吗大脑改善病人的生活质量?
他说:“整个电路还在那里,完好无损。“唯一缺少的就是那些调节过程,这就是治疗的切入点。”
进一步探索