肝脏代谢的微量控制
TIFR的研究人员发现了在肝脏中喂养的分子预期,这是为了确保在禁食后适应身体,适应在再喂食时使用进入的营养。他们的调查结果,在国际期刊上发表细胞报告展示通过抑制蛋白质的合成,表明称为MicroRNAS的非常小的RNA分子控制主要代谢途径,从而有助于维持血糖水平。
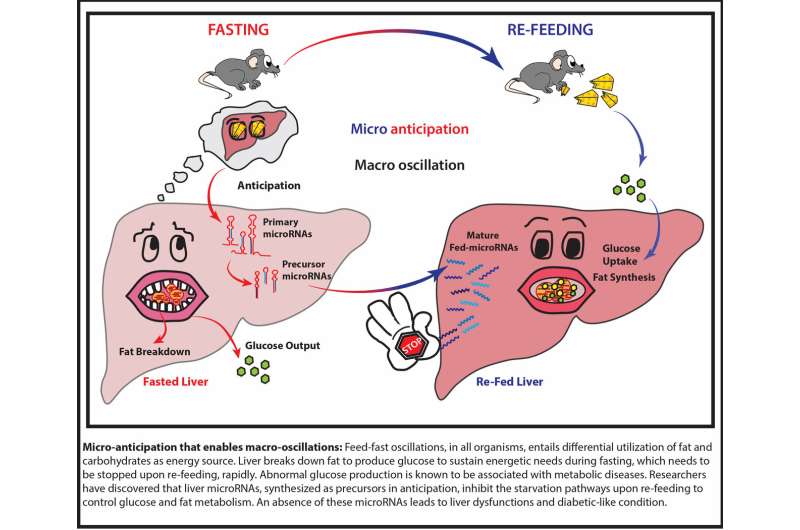
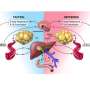
肝脏是中央代谢器官之一,在维持有机体健康和寿命方面发挥着关键作用。全部生物体经过饲料快速循环,其中身体在此期间分解脂肪禁食为了满足能源需求,并在食品消费后使用葡萄糖或碳水化合物。在这些过程之间振荡的不灵活性来自器官(或生物)的失败来切换代谢途径。
已知脂肪或葡萄糖的过度或不利用的含量影响所有生命形式的健康状况。在高度进化的物种中,肝脏作为主要器官来调节脂肪和脂肪葡萄糖新陈代谢并确保既没有过度使用这些能源。已知肝功能困扰与肥胖症和糖尿病有关。异常肝脏代谢是脂肪肝疾病的主要驱动因素之一,这是印度普遍存在的脂肪肝疾病之一。因此,分子机制在肝细胞内带来一个全球变革在禁食到重新进料状态的基因表达中变得至关重要。最近在世界各地的科学家努力飙升,以发现对食物摄入的分子因素(包括日常喂养时间)和昼夜节律(光黑循环),特别是在肝脏中,这影响全身新陈代谢。
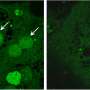
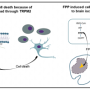
在TIFR进行的研究的关键方面是鉴定“美联储微大罗RNA”的鉴定,其水平在饲养后肝脏增加,停止在禁食期间所需的蛋白质的产生。虽然已知微小RNA对于肝功能很重要,但是最近的发现表明,这些小RNA的特定组起作用在一起以在再喂养时抑制禁食响应。该研究的亮点是发现当小鼠禁食时已经存在这些美联储微小稻草的前体,从而产生预期机制。重要的是,扰动这些美联储微大稻草导致分子和生理变化与血糖水平相关的相关性,让人联想到糖尿病前状态。本研究铺平了使用这些小RNA分子作为控制的潜在治疗目标的方法葡萄糖或脂肪代谢以及作为代谢的合理的干预肝疾病。
进一步探索












用户评论