有前途的化合物选择性地杀死脑癌干细胞
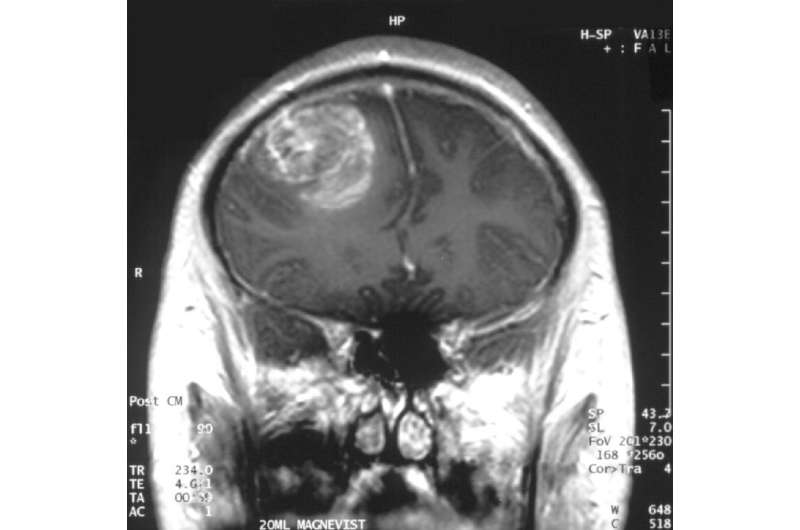
斯克里普斯研究中心的科学家们发现了一种化合物,可以有效地选择性地杀死使胶质母细胞瘤脑癌如此致命的干细胞样细胞。
本周发表在《The美国国家科学院院刊斯克里普斯研究中心的科学家们发现,这种被他们称为RIPGBM的新化合物能够杀死人胶质母细胞瘤从患者肿瘤中培养出的干细胞样细胞,其效力是标准GBM药物的40倍以上temozolomide。他们还发现RIPGBM具有高度选择性,保留了其他类型的大脑它能有效地抑制GBM肿瘤在疾病小鼠模型中的生长。
“我们对这种化合物及其影响的细胞通路的发现为治疗胶质母细胞瘤提供了一个很有前途的新策略,”斯克里普斯研究中心的化学助理教授、首席研究员卢克·莱尔森博士说。
在美国,每年约有1万人被诊断出患有胶质母细胞瘤,而且通常无法治愈,确诊后平均存活时间约为一年。其中包括已故的美国参议员约翰·麦凯恩和爱德华·肯尼迪。
在过去的十年里,科学家们已经看到了胶质母细胞瘤癌症干细胞(GBM CSCs)是这种癌症毒性的关键。GBM CSCs对化疗和放疗具有相对抗性,并倾向于从原发灶迁移肿瘤进入邻近的健康脑组织。因此,即使之后原发肿瘤已经通过手术切除,病人的大脑已经接受了标准的化疗和放射治疗,几乎可以肯定的是,至少有一些已经分散到大脑的GBM CSCs将存活下来,并发展成新的肿瘤。
莱尔森和他的同事们建立了一个自动的大规模筛选测试,其中包含了大约100万个小分子有机物化合物将其应用于普通脑细胞和胶质母细胞瘤患者肿瘤中培养的GBM CSCs。Lairson说:“这些来自患者的肿瘤细胞保留了GBM肿瘤具有侵略性和致命性的特征,包括当注射到小鼠大脑时形成GBM样肿瘤的能力。”
经过几轮筛选,他和他的同事们发现了一种化合物RIPGBM,它能杀死GBM CSCs,同时保留健康的细胞类型。他们发现它的作用如此有选择性是因为它被酶或其他因素修饰,这些因素似乎在GBM CSCs中独特地普遍存在。在这些肿瘤细胞修饰的化合物,cRIPGBM,触发了细胞的自毁过程,称为凋亡。
科学家们发现,在使用人类患者来源的胶质母细胞瘤细胞的标准小鼠模型中,未经治疗的小鼠在五周内发生了通常的大脑瘤,而ripgbm治疗的小鼠则发生了相对较小的脑瘤。
莱尔森和他的同事们计划进一步开发RIPGBM,并进行更多的动物实验——如果一切顺利,最终进行人类临床试验。“原则上,RIPGBM或类似的分子可以极大地降低胶质母细胞瘤肿瘤的再生率,而且副作用很小,因为它可以保护正常的大脑细胞”,Lairson说。
进一步探索

















用户评论