人类微生物代谢物尖端肠道大肠杆菌感染的规模

为什么人类相对容易被一些细菌或病毒病原体感染,而拥有非常相似组织和免疫功能的动物却不会,这仍然是一个谜。这一鸿沟也是为什么研究人员在动物模型(如老鼠)上建模致病性疾病时经常遇到问题的原因,也是为什么使用这种方法开发的药物在人类身上经常失败的原因。
在对肠球中的响应中可以看出对感染耐受性耐受性的特异性特异性差异的醒目例大肠杆菌仅在美国,每年就有超过10万人感染了大肠杆菌(EHEC),它还会导致带血腹泻(旅行腹泻)、结肠炎和溶血性尿毒症综合征(HUS)——这是一种遇到大肠杆菌志贺毒素后导致肾脏衰竭的严重疾病。多年来,人们已经知道,致病性肠出血性大肠杆菌感染小鼠的数量是人类的10万倍,而且小鼠不会出现这种疾病的症状,除非这些动物生长在特殊的无菌条件下,在这种条件下它们缺乏正常的肠道共生微生物群。
在哈佛大学的生物工程师,微生物学家和系统生物学家中的多学科团队,在哈佛大学的Wysss生物学启发工程研究所,在研究所的DARPA支持的“主持人恢复能力”(Thor)项目中,其目标是揭示宽容的原因对某些个体或物种表现出的感染,现在已经成功地建模了人类感染冒号使用Mehec使用微流体器官芯片(器官芯片)培养装置。令人惊讶的是,它们的方法使得鉴定了由聚合物细菌的复杂群落产生的代谢物之间的关键差异,其包含在小鼠与人结肠中存在的微生物组。他们发现,人体肠道微生物组在更高水平下产生的四种代谢物可以帮助解释人结肠对EHEC的增强敏感性。这项研究发表在微生物组。
“我们的动机是观察到,当受到同样的病原体攻击时,人类和老鼠肠道的敏感性往往存在巨大差异,过去的工作已经表明,这些对感染的耐受性的一些差异可以用这些物种之间的肠道微生物群的差异来解释,”Wyss研究所创始主任,领导这项研究的医学博士、博士唐纳德·因格伯说。“为了直接解决这个问题,我们利用了我们的人体器官芯片技术,并将其与生物反应器产生的微生物代谢物结合,以及代谢组学分析,以深入了解这种物种对肠出肠杆菌敏感性差异的分子基础。”Ingber还是哈佛医学院(HMS)的Judah Folkman血管生物学教授和波士顿儿童医院的血管生物学项目教授,以及哈佛大学约翰A.保尔森工程与应用科学学院的生物工程教授。
由于EHEC主要感染人类结肠,因此该团队首先使用其微流体培养技术组装结肠芯片,并利用其最近使用称为有机体的肠组织片段作为产生自发形成手指状的高功能肠上皮的中间体的肠组织片段在设备中称为肠绒毛的预测。在结肠芯片中,通过涂覆有细胞外基质(ECM)的多孔膜(ECM)分离的两个平行通道(“肠腔通道”)中的一种结肠上皮线。相对的通道(“血管通道”)由人肠内加管细胞排列,所述人肠内加管细胞模仿血管支撑和与结肠上皮进行连通。
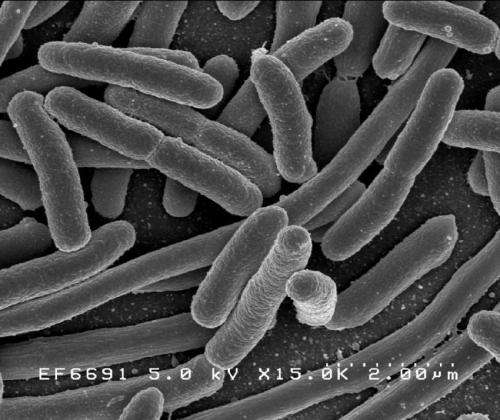
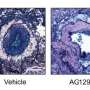
该团队测试了由复杂小鼠和人类微生物群落中产生的可溶性分子的全部复杂性是否在生物反应器中培养的,其模仿大肠内部环境不同地影响人性结肠芯片中的EHEC感染性。“在加入人微生物组特异性代谢物后,人性结肠上皮患者严重损伤,随着细胞死于组织的细胞和脱离组织,而暴露于小鼠微生物组特异性代谢物的相同的人性上皮较小,“第一作者Alessio Tovaglieri在瑞士欧洲埃特·苏黎世的一名学生上演出了他的毕业生。“有趣的是,病原体eHEC细菌在没有微生物组代谢物的情况下没有损伤结肠组织,并且复杂的代谢物混合物本身在没有EHEC的情况下没有任何影响。”
该团队能够证明,人类和小鼠微生物组代谢物引发的损伤差异不是由于炎症细胞因子的变化、志贺毒素产生的差异或肠出血性大肠杆菌定植结肠上皮细胞能力的改变。为了更接近真正的根本原因,他们进行了转录组学分析,分析了暴露于人类和小鼠微生物组代谢物后肠出肠大肠杆菌基因表达的变化,并进行了代谢组学分析,以确定两种代谢物混合物的化学成分差异。
“编码在EHEC趋化性和鞭毛运动中起作用的蛋白质的基因在由人微生物组的代谢物特异性上调的所有基因中均有最高的,似乎增强致病性,并且有趣的是,我们发现暴露于人类微生物组的代谢物的EHEC细菌更具动机,“Tovaglieri说。鞭毛是许多细菌使用像电机的复杂细长的附属物,使自己朝向食物来源(趋化性)。
在这两种代谢物混合物中,有426种代谢物以不同的水平存在,其中四种人类微生物组代谢物的组合,它们的水平都高于它们在小鼠微生物组中的水平,足以增加培养皿中肠出血性大肠杆菌的运动性。重要的是,它们也足以转化正常无害的小鼠微生物组代谢物混合物进入促进人结肠芯片装置中对结肠组织的损害的一种,使其作为人微生物组的代谢物有效。一些相同的代谢产物被发现在尚不清楚儿童对EHEC感染更敏感的情况下。
“这项工作已经发现,如果我们能够开发抑制其生产或增强人类的患者,可以帮助减轻患者患者的潜在分子靶标。相同的人体芯片方法与代谢组合相结合,可以帮助识别介导的其他代谢物未来对其他感染的保护作用和增加耐受性。它还可以帮助我们进一步了解为什么某些人对感染敏感的原因,而其他人则宽容,“夹木说。
进一步探索









用户评论