在分子水平上,癌症突变与达尔文的观察结果相呼应
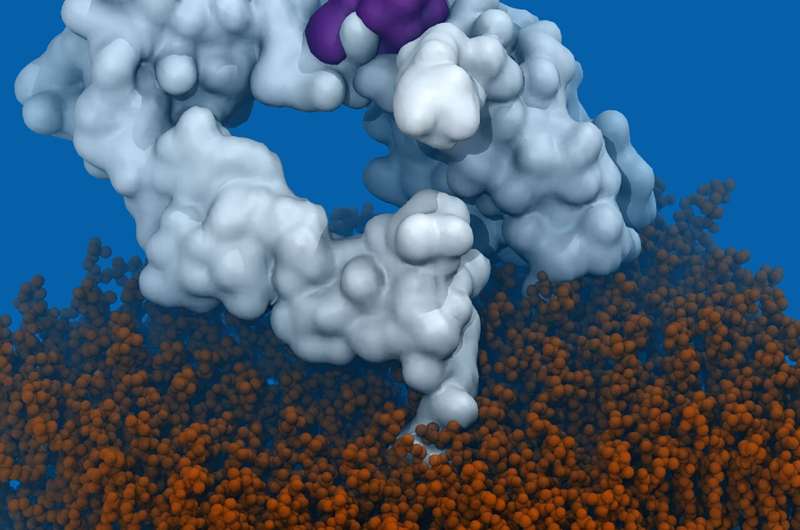
致命脑癌背后有100多种蛋白质突变,但胶质母细胞瘤,但是国际研究团队发现了这些突变的共同点。新的理解可能导致对不同种类的癌症进行更有效的治疗方法。
该研究由斯德哥尔摩皇家理工学院的研究人员劳拉·奥雷拉纳领导,该研究揭示了新的问题表皮生长因子受体(EGFR)与胶质母细胞瘤(GBM)相关的基因,一种可治区的形式大脑以及抗体mAb806的成功。该抗体是由路德维希癌症研究所(LICR)开发的,用于治疗大量的突变,远远超过迄今为止批准的两项应用。
使用计算模拟Orellana发现,一些GBM突变去除了蛋白质的抑制部分,而另一些则取代了它,因此EGFR可以在没有生长信号的情况下发挥作用。“当蛋白质从非活性状态转变为活性状态时,它们都获得了一种中间形状,”她说。令人惊讶的是,这种蛋白质形状的变化暴露了通常被“埋藏”的蛋白质区域,这是mAb806的靶点。
“以简单的话语,显然不同的突变达到相同的效果,激活EGFR在脑环境中生长,这导致暴露Achilles脚跟,这可能幸运地被MAB806封锁,”Orellana说。
国际研究包括来自Licr San Diego的研究人员,该研究人员确认了携带胶质母细胞瘤突变的肿瘤对脑癌小鼠模型中的MAB806治疗的计算预测。结果也有助于理解为什么GBM突变与酪氨酸激酶抑制剂(TKI)的广泛使用的抗癌药物相同的响应,允许其与MAB806的合理组合即使在非突变细胞中也可以实现肿瘤回归。
Orellana指出了这些调查结果的相似性与收敛演变的理论,其中不同种类适应普通环境,哺乳动物如海豚和鲸鱼的方式与类似鱼类类似的翅片演变。“在脑癌的情况下,细胞进化了许多不同的EGFR突变,但它们都导致了类似的形状,可以由同一药物瞄准,“她说。
Orellana的研究是在她在Kth和斯德哥尔摩大学工作的博士后工作。
这项研究发表在美国国家科学院院刊(pnas.)。
“这是趋同进化的一个非常有力的证明癌症,它极大地扩展了mAb806的频谱,超过了迄今为止已经批准的两个应用,”她说。
进一步探索











用户评论