研究人员揭示了ALS的新治疗策略
神经科学研究所的研究人员及其合作者揭示了肌萎缩性侧索硬化症(ALS)的一种新的细胞机制,提出了一种针对RNA降解途径的新的治疗策略,并确定了一种哮喘药物作为治疗ALS的潜在药物。
在网上发表的一项研究大脑4月1日,来自中国科学院神经科学研究所徐进博士实验室的研究人员及其合作者揭示了一种新的细胞机制肌萎缩性侧索硬化症(ALS),建议写一本小说治疗策略以RNA降解途径为目标,并确定了一种哮喘药物作为治疗ALS的潜在药物。
ALS是最常见的运动神经元疾病,也是最具破坏性的疾病之一神经退行性疾病由进行性运动神经元变性引起。这种疾病无法治愈,目前的治疗方案非常有限。因此,该病的特点是进展快,致死率高。
最近的遗传学进展已经确定了一组新基因,它们的突变有助于ALS的发展。在这些基因中,C9orf72是家族性渐冻症最常见的遗传原因,甚至有助于偶发性渐冻症的发生。
与常见的点突变和缺失不同,C9orf72非编码区(GGGGCC)n六核苷酸重复序列扩增(HRE)是罪魁祸首。有趣的是,这些重复序列可以产生RNA和蛋白质产物,并像其他一些引起als的突变蛋白一样影响RNA代谢,尽管其潜在机制仍有待完全了解。
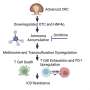
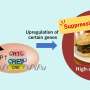
在本研究中,通过将各种转录组研究的无偏生物信息学分析与多个C9orf72细胞和动物模型的验证实验相结合,徐博士的团队揭示了对无意义介导的mRNA衰减(NMD)通路的抑制是C9orf72 HRE的保守结果。
NMD是一种RNA监测机制,对于清除由错误转录、替代剪接或病毒感染产生的缺陷或有害RNA至关重要。NMD的关键蛋白质成分存在于被称为加工体的细胞质结构中。
有趣的是,研究人员发现hre衍生的神经毒性二肽重复序列(DPRs)可以通过抑制加工体形成而促进应激颗粒形成来抑制NMD途径。
为了测试NMD通路是否可能成为ALS的潜在治疗靶点,他们首先从基因上重新激活了NMD通路并发现核心NMD基因,如UPF1,可以有效地保护C9orf72 DPRs神经毒性。接下来,在评估了几种潜在的nmd激活化合物后,他们认为Tranilast是最有前途的nmd激活药物,并发现它可以从C9orf72 dprd诱导的神经毒性中拯救细胞和果蝇。
鉴于自20世纪80年代以来,经血脑屏障渗透的曲尼司特已被临床用于治疗哮喘,并具有良好的安全记录,本研究将促进未来的临床前和临床研究,以测试曲尼司特和其他nmd激活化合物对RNA代谢缺陷的ALS患者的治疗潜力。