一个全面的阿尔茨海默氏症如何影响大脑的地图
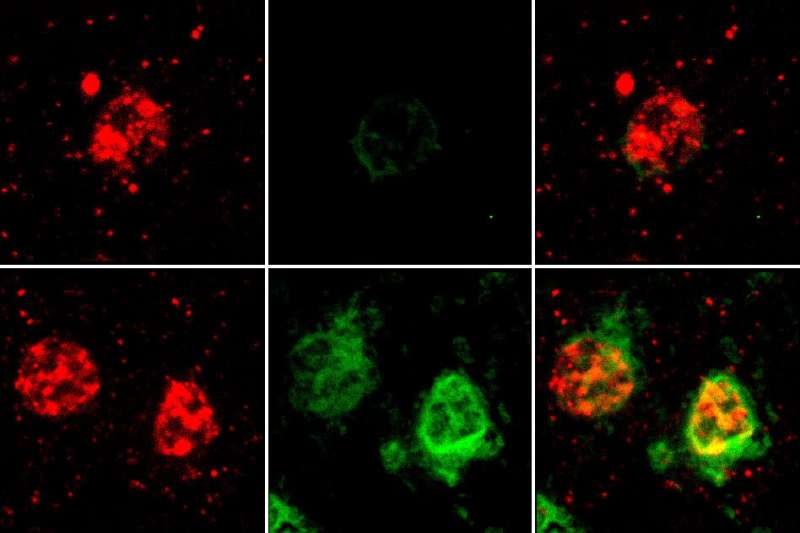
麻省理工学院的研究人员已经完成了第一个综合分析基因表达的个别脑细胞的阿尔茨海默氏症患者。结果允许团队识别独特的细胞通路影响大脑和其他类型的神经元细胞。
这种分析可以提供许多潜在的新的阿尔茨海默氏症的药物靶点,折磨超过500万人在美国。
“这项研究提供了,在我看来,第一个地图会在所有的分子过程中改变阿尔茨海默氏症在每一个细胞类型,我们现在可以可靠地描述,“Manolis凯利斯说,教授计算机科学和麻省理工学院计算机科学和人工智能实验室和广泛的麻省理工学院和哈佛大学。“它打开了一个全新的时代对于理解阿尔茨海默氏症”。
这项研究显示,这一过程被称为轴突髓鞘形成明显影响患者的阿尔茨海默氏症。研究人员还发现,大脑细胞在他们上的男人和女人有很大的不同基因应对疾病。
麻省理工学院的主任因数和Li-Huei蔡Picower研究所学习和记忆,这项研究的资深作者,发表在5月1日在线版自然。麻省理工学院博士后所长Hansruedi数学和何塞Davila-Velderrain是论文的主要作者。
单细胞分析
研究人员分析了后期大脑样本24人表现出高水平的阿尔茨海默病病理和24年龄相仿的人没有这些疾病的迹象。所有的受试者研究宗教团体的一部分,衰老和老年痴呆症的纵向研究。研究人员也对受试者的数据在认知测试中的表现。
麻省理工学院的团队对约80000个细胞进行单细胞RNA序列从这些科目。先前的研究基因表达在老年痴呆症患者的整体RNA水平测量的部分大脑组织,但这些研究不区分细胞类型,它可以掩盖的变化发生在更丰富的细胞类型,蔡说。
“我们想知道如果我们能区分每个细胞类型之间差异基因表达模式健康和患病的大脑组织,”她说。“这是单细胞水平的力量分析:你有决议真的看到所有不同的细胞类型之间的差异在大脑。”
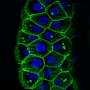
使用单细胞测序方法,研究人员能够分析不仅最丰富的细胞类型,包括兴奋性和抑制性神经元,但也少见,non-neuronal脑细胞如少突胶质细胞、星形胶质细胞和小胶质细胞。研究人员发现,这些细胞类型显示不同的基因表达差异在老年痴呆症患者。
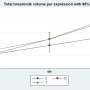
一些最重要的变化发生在轴突再生和髓鞘形成相关的基因。髓磷脂是一种脂肪鞘,使轴突,帮助他们来传输电信号。研究人员发现,患有老年痴呆症,髓鞘形成相关基因影响神经元和少突胶质细胞,这些细胞产生髓磷脂。
细胞类型特异的基因表达的变化这些疾病发生发展的早期。在以后的阶段,研究人员发现,大多数细胞类型有非常相似的基因表达模式的改变。具体地说,大多数脑细胞出现应激反应相关的基因,细胞程序性死亡,维持蛋白质所需的细胞机制的完整性。
性别差异
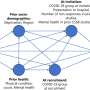
研究者还发现基因表达模式之间的相关性和其他措施的阿尔茨海默氏症严重程度等淀粉质色斑和神经元纤维缠结的程度,以及认知障碍。这使他们能够识别“模块”的基因似乎与疾病的不同方面。
“识别这些模块,我们设计了一个新策略,包括使用一种人工神经网络,它让我们了解基因的集合与阿尔茨海默病的不同方面在一个完全公正,数据驱动的方式,“数学说。“我们预计,这一战略还将有价值的确定基因模块与其他大脑疾病有关。”
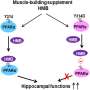
最令人惊讶的发现,研究人员说,发现的显著区别的从男性和女性的老年痴呆症患者大脑细胞。他们发现兴奋性神经元和其他男性病人的大脑细胞显示不明显比细胞基因表达的改变阿尔茨海默氏症女性个体,尽管这些患者出现类似症状,包括淀粉样斑块和认知障碍。相比之下,女性患者的大脑细胞显示显著更严重阿尔茨海默病的基因表达变化,和一组扩展的路径改变。
“当我们意识到有一些非常有趣的。我们感到很震惊,”蔡说。
到目前为止,尚不清楚这种差异存在的原因。少突胶质细胞的性别差异尤其明显,产生髓磷脂,所以研究人员进行分析病人的白质,主要有髓鞘的轴突组成。使用一组核磁共振扫描从500年宗教团体的其他科目学习小组,研究人员发现,女性受试者与严重的记忆缺陷白质损伤比匹配的男性受试者。
需要更多的研究来确定为什么男人和女人的反应如此不同的阿尔茨海默氏症疾病,研究人员说,这些发现可能会对发展中国家和选择的治疗方法。
“有越来越多的临床和临床前阿尔茨海默氏症倾向的两性异形的证据,但没有已知的潜在机制。我们的工作指出微分细胞过程涉及non-neuronal髓鞘细胞具有潜在的作用。要弄清楚这些差异的关键保护或损害大脑细胞只在其中一个性别和如何平衡响应所需的方向,”Davila-Velderrain说。
研究人员目前正在用老鼠和人类诱导多能干细胞模型进一步研究的一些关键细胞通路,他们确定为与阿尔茨海默氏症在这项研究中,包括那些参与髓鞘形成。他们还计划执行类似的基因表达分析相关的其他形式的痴呆阿尔茨海默氏症,以及其他大脑疾病如精神分裂症、双相情感障碍,精神病,多样化的痴呆症。