年龄本身似乎增加了大脑中阿尔茨海默氏症的蔓延
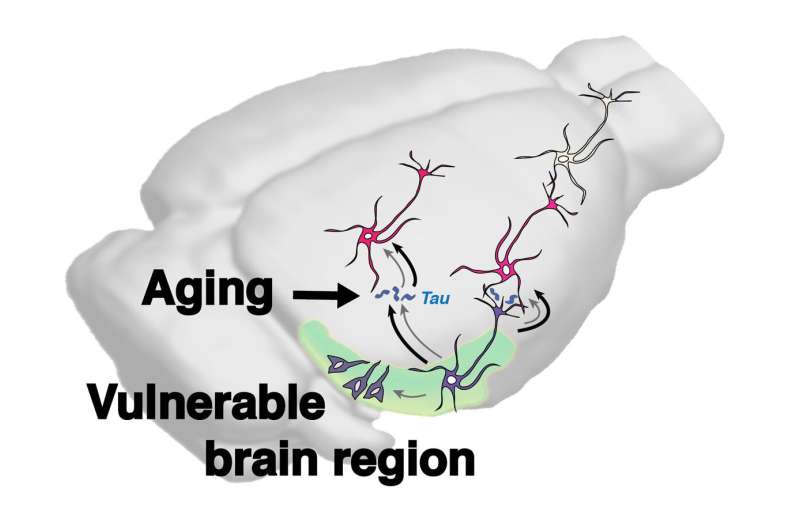
Massachusetts综合医院(MGH)的调查人员发现了通过老化大脑本身的因素促进了Alzheimer的相关蛋白质TAU的脑力的证据,而不是蛋白质已被神经元表达的长度。他们的报告发表在科学推进设定研究阶段,以确定这些因素,又可以导致新的治疗策略。
“零星的阿尔茨海默病和其他神经退行性疾病的事实是明显的,但原因是未知的原因,”全能神经退行性疾病(Mass Generogenerative疾病)的Alzheimer的部门主任Bradley Hyman,Ph.D。本文的高级作者。“现有的动物模型,如突变的小鼠,突然突发出来,以延长含有陶氏缠结的缠结,不能区分动物的年龄或大脑的寿命暴露于增加的TAU,这是对病理学作用的原因。“
为了克服这一限制,海曼的团队 - 包括领导和与联合同学作者Susanne Wegmann,博士,现在在德国神经退行性疾病研究所 - 开发了一种病毒基因载体,诱导人类的病理或正常形式的表达。载体还将荧光标签应用于直接表达TAU的神经元,从而能够从包含从相邻细胞传播的TAU的神经元的分化,这可能反映了Alzheimer的Tau病理学如何通过大脑传播。
研究人员首先证实,将载体引入Entorhinal Cortex(EC) - 该脑结构如果阿尔茨海默氏症相关的Tau病理学首次出现的小鼠可以诱发人体Tau的表达和传播,然后它们使用载体诱导肌肉中的被错误的病理学或未传统形式的EC中的表达,发现了,而存在Tau对相邻细胞的扩散不需要错误折叠的蛋白质,在被错误折叠的TAU诱导时,扩散更快,更广泛。
比较诱导牙龈大脑病理形式的表达的效果显示,从EC到相邻地区的差异率大约是较老小鼠的两倍,这也积累了更具错误的TAU年轻的动物。然而,当将载体引入纹状体神经元时,没有看到诱导的Tau表达的相同效果,这很少在阿尔茨海默病患中受到影响。
“虽然年龄是阿尔茨海默氏症的最高的非遗传危险因素,直到现在,它尚未测试是否自身的年龄可以使大脑容易受到对土地的病理变化和传播的大脑,”Wegmann说。“现在我们和他人需要努力解决衰老的脑子为Tau传播的更好平台以及决定某些脆弱性的问题脑地区。“
哈佛大学医学院神经内科教授的Hyman补充道,“我们希望更多地学习关于如何生理的老龄化脑有助于开发阿尔茨海默病将导致许多人的预防性和治疗选择神经退行性疾病。“
进一步探索











用户评论