分解病理性蛋白质聚集物

ETH研究人员发现了一种新的机制,脑细胞用来保护自己不受蛋白质聚集的影响。这些聚集物在帕金森氏症和其他神经退行性疾病中起着关键作用。这个新发现可能为新的治疗方法提供基础。
突触核蛋白在神经细胞中的聚集大脑在帕金森氏症和其他疾病中起着关键作用神经退行性疾病。这些蛋白质团块可以从一个神经细胞转移到另一个神经细胞,导致疾病的进展。由ETH科学家领导的研究团队现在发现了人体如何清除这些有害的聚集体。他们的发现可能为治疗神经退行性疾病开辟新的途径。
与这些疾病相关的是长而微的纤维或原纤维,大量的α -突触核蛋白分子可以聚集在这些纤维上。然而,个体、非聚集的α -突触核蛋白分子是健康大脑功能的关键,因为这种蛋白质在神经细胞突触释放神经递质多巴胺中起着关键作用。当蛋白质聚集在人的神经细胞变成原纤维之前,它必须先改变它的三维形状,它不能再执行它的正常功能。纤维对神经细胞也是有毒的。反过来,产生多巴胺的细胞死亡,导致大脑多巴胺供应不足,导致典型的帕金森症临床症状,如肌肉震颤。
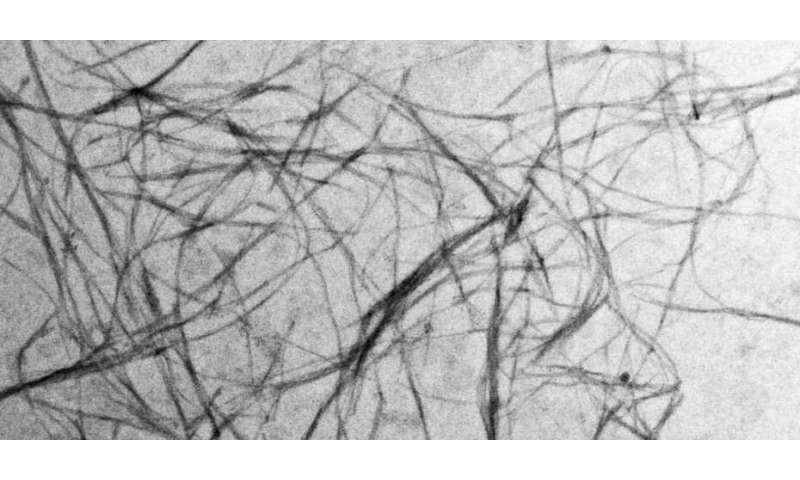
击穿机制破译
通过细胞培养实验,研究人员能够证明是α -突触核蛋白原纤维可以进入健康细胞并在这些细胞中积累。“一旦这些原纤维进入一个新的细胞,它们‘招募’那里的其他α -synuclein分子,然后改变它们的形状并聚集在一起。”这就是纤丝被认为如何一个接一个地感染细胞,并随着时间的推移接管整个大脑区域,”苏黎世联邦理工学院蛋白质网络生物学教授Paola Picotti解释说。她构思了这项研究,并发表在最新一期的杂志上科学转化医学该研究由她团队中的前博士后胡安·热雷斯(Juan Gerez)领导。
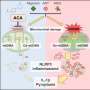
来自苏黎世联邦理工学院、苏黎世大学医院和加州大学圣地亚哥分校的科学家团队还破译了一种自然分解α -突触核蛋白原纤维的细胞机制。一个蛋白质复合体这种被称为SCF的物质能够特异性地检测到α -synuclein原纤维,并将其定位于一种已知的细胞分解机制。通过这种方式,原纤维的扩散被阻断,正如研究人员在小鼠实验中所证明的那样:当研究人员关闭SCF的功能时,神经细胞中的α -突触核蛋白原纤维不再被清除。相反,它们在细胞中积累并扩散到整个大脑。
干细胞或基因治疗
Picotti和Gerez认为,这种SCF破裂机制在治疗中有很好的应用前景。Gerez说:“SCF复合物越活跃,α -synuclein原纤维被清除得越多,这可能会减缓或最终阻止这类神经退行性疾病的进展。”他继续解释道,SCF复合体非常短暂,几分钟内就会消散。治疗方法将集中于稳定复合物和提高其与α -synuclein原纤维相互作用的能力。例如,可以为此目的开发药物。
另一种帮助帕金森氏症患者的方法是移植神经就像皮科蒂说的那样。她解释说,之前的尝试并不是很成功,因为α-突触核蛋白大脑中的原纤维感染了健康人细胞。“如果我们能设法修改干细胞通过这样的方式,他们要么不让原纤维进入,要么立即分解它们允许进入的原纤维,这可以促进干细胞治疗。”她总结道。最后,基因治疗可以用来稳定SCF复合体神经细胞从而增加它的活性。“然而,当谈到潜在的治疗方法时,我们还处于起步阶段,”Gerez说,“是否能开发出有效的治疗方法还不清楚。”
进一步探索










用户评论