分拣蛋白在神经元保护对神经退行性疾病

像分拣机在装配线,分子被称为VPS35检测并移除缺陷从神经元蛋白质。和类似于其他质量控制流程,VPS35系统对保护人类健康,根据研究人员的新工作刘易斯卡茨在天普大学医学院。他们第一次展示VPS35清除大脑潜在有害的蛋白质叫做τ,否则积累,导致神经退行性疾病,包括阿尔茨海默氏症。
新的研究结果在线发表在《华尔街日报》7月9日《分子精神病学》。
“什么VPS35的主要部分是整理和运输功能失调的蛋白质降解网站,“解释高级调查员Domenico Pratico,医学博士,斯科特·理查兹北极星阿尔茨海默氏症研究基金会主席药理学和微生物学教授,阿尔茨海默病中心主任寺庙刘易斯Katz医学院(LKSOM)。
缺陷蛋白在神经元特性的形成共享的阿尔茨海默氏症,帕金森氏病,和其他几个神经退行性条件。τ是一个主要的蛋白质积聚的大脑在这些疾病造成损害,创建一个称为tauopathy条件。
之前的工作由其他研究人员已经表明VPS35的功能是改变在阿尔茨海默病和VPS35活动是减少老年痴呆症患者的大脑中。VPS35活动和τ积累之间的关系很大程度上是未知的。
“我们要求专门为清算VPS35系统是否重要缺陷tau蛋白质,“Pratico博士说。要回答这个问题,他的研究团队研究了从患者脑组织进步supra-nuclear麻痹(PSP)或选择的疾病。与阿尔茨海默病,τ是次要的β-淀粉样蛋白的积累,在PSP和τ是唯一选择的疾病蛋白质在大脑中形成的存款。
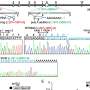
分析表明,PSP和挑选的疾病患者的大脑VPS35水平比对照组低50%。当研究人员故意改变VPS35水平个人tauopathy-affected神经元在体外,他们发现他们可以直接控制τ积累,首次暗示VPS35 tauopathy。τVPS35-dependent效应是由活动的组织蛋白酶D,专门从事蛋白质降解酶。
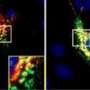
Pratico博士的研究小组还进行了实验小鼠τ积累。在这些动物差别VPS35对这些加剧了记忆和学习障碍和运动机能恶化有关。此外,VPS35减少导致神经元之间的突触失去完整性的动物的大脑,大大损害神经沟通。
“当τ徘徊在细胞,是非常糟糕的突触,神经元的地方见面和交流信号,“Pratico博士解释说。“在我们研究的动物,有40 - 50%的损失在突触连接VPS35活动减少,导致认知和运动恶化的类型,包括损失在记忆和学习能力,在人类tauopathy病人。”
的发现的参与组织蛋白酶D揭示VPS35之间的关系和额外的τ。“没有VPS35,组织蛋白酶D不降低τ,τ建立在大脑中,留下“Pratico博士说。
Pratico博士的研究小组计划下一个调查的可能性,使用药物来让VPS35重返工作岗位在神经退行性疾病。“方法是独一无二的。而不是针对一种酶,其他小分子已经开发出来,我们会针对一个实际的机制,应该更可行的,”他说。