研究揭示了干细胞移植排斥的新线索

2006年,科学家们发现了一种将成熟细胞(例如成年皮肤细胞)“重新编程”成干细胞的方法,这种干细胞原则上可以分化成人体的任何组织或器官。许多人认为,这项突破性的技术进入临床并开启再生医学革命只是时间问题。
因为同一个病人既是供体又是受体细胞源自这些所谓的诱导多能干细胞(iPSCs),这些细胞将被视为“自我”免疫系统他们的想法是这样的,而且不受传统移植所面临的排异问题的影响。
但由于不可预见的挫折,包括ipsc衍生的令人惊讶的临床前发现,ipsc并没有成为最初设想的万灵药细胞移植它们经常被排斥,即使在重新引入细胞来源的有机体之后。
科学家们一直在努力理解这种排斥发生的原因。但是,加州大学旧金山分校移植和干细胞免疫生物学(TSI)实验室与美国国家心肺血液研究所(NHLBI)和斯坦福大学的移植基因组学实验室合作进行的一项新研究表明,成人到ipsc的转换过程可以突变被称为线粒体的微小细胞结构中的DNA。这些突变会引发免疫反应,导致小鼠和人类排斥iPSCs,更普遍的是排斥干细胞移植。
“在再生医学领域,线粒体的作用在很大程度上被忽视了,但我们实验室早期的努力表明,它们可能会影响干细胞移植的结果,”加州大学旧金山分校Julien I.E. Hoffman心脏外科主席、新研究的主要作者、医学博士Tobias Deuse说自然生物技术.“重要的是,我们要了解它们的作用,这样我们才能可靠地控制我们的工程细胞的质量,并确保干细胞产品可以移植到患者体内而不产生排斥反应。”
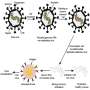
线粒体通常被称为细胞的动力源,它产生的能量为地球上几乎所有的生物过程提供燃料(没有线粒体的细菌是例外)。但线粒体的特殊之处在于另一个原因:它们包含自己的基因组。
“核”人类基因组,因为它存在于细胞核中,包含超过2万个蛋白质编码基因和30亿个DNA碱基——构成遗传密码的四字母化学字母表。相比之下,人类线粒体基因组只包含13个蛋白质编码基因和不到17000个碱基。然而,在高能量需求的组织中,微小的线粒体基因组可以不成比例地贡献细胞的总蛋白质含量。
“在做大量工作的细胞中,如心肌细胞,高达三分之一的细胞产生蛋白质的mRNA分子来自线粒体。这意味着单个线粒体突变的负担可能是巨大的。你不会只得到几个可能引发免疫反应的蛋白质——你会得到数千个,”外科教授、新研究的资深作者、医学博士Sonja Schrepfer说。
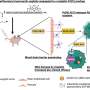
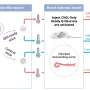
为了证明这种线粒体突变可以引发免疫反应,科学家们用一种小鼠品系的细胞核DNA和另一种小鼠品系的线粒体DNA创造了混合干细胞。他们将这些细胞移植到核DNA相同的小鼠体内,但这些小鼠的线粒体DNA在两个蛋白质编码基因中有一个碱基的差异。移植几天后,他们从小鼠身上收集免疫细胞,并将这些细胞暴露在各种线粒体蛋白质片段中。唯一引起反应的蛋白质是由两个“外来”线粒体基因产生的蛋白质。
虽然类似的实验不能在人类身上进行,但科学家们能够设计出一个巧妙的变通办法。“我们招募了肝和肾移植患者,并设计了利用捐赠者和接受者线粒体DNA中自然发生的序列差异的实验,”Deuse说。
与小鼠实验一样,研究人员从每个移植受者身上分离出免疫细胞(本例为3个月和6个月后),并将细胞暴露于线粒体蛋白质片段。结果是一样的:受体的免疫细胞只被来自器官供者的“外来”线粒体蛋白质触发。
Schrepfer说:“在老鼠和人类中,即使是一个线粒体突变也足以产生可识别的免疫反应。”
但一个重要的问题仍然存在:ipsc衍生细胞的行为是否与肝和肾细胞相同?
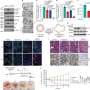
Deuse说,事实证明iPSC转化过程是高度诱变的,并导致许多新的、激活免疫的线粒体突变。“在正常生理条件下,线粒体DNA比核DNA更容易发生突变10到20倍。将成年细胞转化为干细胞是一个艰难的过程,所以我们预计突变率会一样高,甚至更高。”
此外,与细胞核不同,线粒体缺乏修复DNA的分子机制。相反,身体依靠免疫系统找到并摧毁产生不熟悉的线粒体蛋白质的细胞——这是线粒体DNA发生突变的明显迹象。
但是,Shrepfer说,成为iPSCs的细胞经过重新编程并在体外生长,不经过免疫系统的清除过程。“我们不是在有机体中制造iPSCs,我们是在没有免疫监视的培养皿中制造它们。我们培养这些细胞的时间越长,引入新的突变的可能性就越大,或者已经存在的非常罕见的突变被放大的可能性就越大。这使得iPSCs在移植时更容易被排斥。”
该研究的合著者,医学博士Hannah Valantine的实验室进行了基因测序,以确定这些线粒体DNA突变,她说,这些发现可能会对移植领域产生重大影响。
国家卫生研究院下属的NHLBI心血管分支器官移植基因组学实验室的首席研究员Valantine说:“这项研究揭示了移植排斥的一种可能的新机制,这可能在未来被用来开发更好的诊断和免疫抑制剂。”
但是iPSC移植并不是注定的,Deuse和Schrepfer说之前发现的一种方法万能“隐形”这一技术可以确保iPSCs和其他干细胞线粒体突变不会被排斥。但如果没有这种隐形斗篷,新的研究表明,临床医生可能需要在实施干细胞疗法之前对线粒体突变进行仔细的筛选。
“底线是我们想让人们意识到这一现象。仅仅因为iPSCs来自于你自己的细胞并不一定意味着它们不会诱发免疫反应Schrepfer说。“在iPSC生产过程中很容易引入突变,因此在移植之前对用于治疗的iPSC和干细胞产品进行线粒体突变筛选是至关重要的。”