破解胰腺癌的入侵和逃避策略
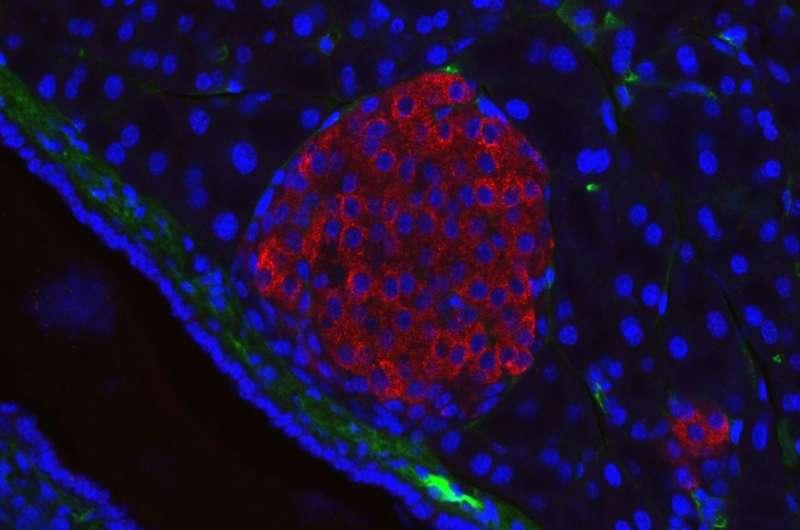
两种已知的基因突变可诱导途径增强胰腺癌侵袭组织和逃避免疫系统的能力。研究人员报告了这一过程的分子细节,为免疫治疗的药物靶点提供了见解。
KRAS和TP53基因的突变与胰管腺癌密切相关,而胰管腺癌是目前最常见的胰腺癌类型。胰腺癌在确诊时通常已经是恶性的了,这使得它的五年存活率极低——不到10%。因此,了解它是如何在分子水平上进化的,将有助于抗癌药物的开发。
日本北海道大学的Hisataka Sabe及其同事在人类癌细胞和该疾病的小鼠模型中进行了试验,以研究KRAS和TP53基因突变在胰腺导管腺癌中的作用。该研究发表在该杂志上美国国家科学院院刊(PNAS)。
他们发现KRAS的突变增加了两种蛋白质ARF6和AMAP1的产生,他们之前发现这两种蛋白质构成了信号传导通路参与癌细胞的侵袭和恶性肿瘤。
基因TP53的突变也被发现促进ARF6的激活,除了引起a代谢途径,被称为甲羟戊酸途径,进入超速运行。这一途径因其增强某些癌症侵袭性的作用而为人所知。
对ARF6-AMAP1通路的进一步研究发现,它参与促进癌细胞上一种名为PD-L1的免疫检查点蛋白的细胞表面表达,除了增强其在细胞内的循环。PD-L1在癌细胞上的表达帮助它们隐藏免疫系统,避免攻击。突变的KRAS和TP53基因,以及甲戊酸途径的过度激活,都在PD-L1的最终细胞表面表达和再循环中发挥了关键作用。
“我们发现,两种已知的胰腺癌驱动突变可以通过促进ARF6通路促进对其他组织的侵袭和对免疫系统的逃避。这意味着恶性肿瘤可能与肿瘤发生并行发展,使得在早期阶段检测癌细胞变得困难,”Hisataka Sabe说。“还需要进一步的研究来确定PD-L1参与免疫逃避的程度。研究还需要考虑PD-L1-和arf6靶向药物是否可以制造胰腺癌症细胞更容易受到免疫系统的攻击,”他继续说。
进一步探索








用户评论