对小鼠的研究确定了与口吃有关的脑细胞类型
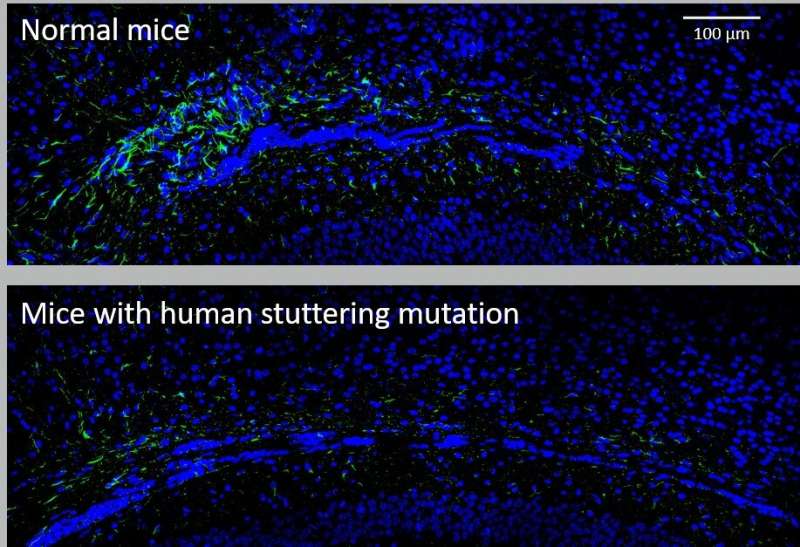
研究人员认为,口吃——一种潜在的终生的、使人衰弱的语言障碍——源于控制语言的大脑回路的问题,但这些问题究竟是如何发生的以及在哪里发生的还不清楚。通过一个口吃的小鼠模型,科学家报告说,大脑中星形胶质细胞的损失与口吃有关。这些小鼠被植入了一种与口吃有关的人类基因突变。这项研究发表在美国国家科学院院刊,提供了与口吃相关的神经缺陷的见解。
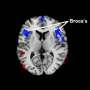
星形胶质细胞的丧失,星形胶质细胞是脑中的支持细胞大脑大脑胼胝体是连接两个半球的大脑部位。之前的成像研究已经发现了口吃者与非口吃者的大脑差异。此外,其中一些对人的研究也揭示了与对小鼠的新研究相同的大脑区域的结构和功能问题。
这项研究是由Dennis Drayna博士领导的,他是美国国家耳聋和其他交流障碍研究所(NIDCD)交流障碍遗传学部门的一员,该研究所隶属于美国国家卫生研究院。圣路易斯华盛顿大学医学院、国家卫生研究院国家生物医学成像和生物工程研究所以及国家心理健康研究所的研究人员合作进行了这项研究。
“对导致口吃的基因、分子和细胞变化的识别,使我们将持久性口吃理解为一种大脑疾病,”NIDCD科学主任安德鲁·格里菲斯(Andrew Griffith)说。“也许更重要的是,精确定位大脑区域和细胞这为口吃和其他语言障碍的新干预提供了机会。”
口吃的特征是停顿和重复或长时间的声音、音节或单词,这打乱了正常的说话流程。口吃的人知道他们想说什么,但他们说出来有困难。这种情况最常见的是在长大后通常会克服这种问题的幼儿身上。然而,对于四分之一经历早期口吃的儿童来说,这种情况会成为终生的沟通问题。据估计,在美国有多达1%的成年人受到口吃的影响。
德雷纳说:“对口吃者的大脑成像研究很重要,但这些结果只能让我们走到这里。”他说,一个挑战是,影像学研究无法解释这些差异是导致口吃的原因还是口吃的结果。
“通过采用遗传方法,我们已经能够开始破译口吃的神经病理学,首先在分子水平上通过识别基因突变现在是在细胞水平,”德雷纳补充说。
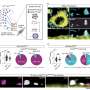
德雷纳和他的同事早期的研究已经确定了几个与口吃有关的基因。在这项研究中,研究人员开始识别由突变在一种名为GNPTAB的基因中,这是一种之前与口吃有关的基因。科学家们将这种人类口吃突变基因改造成老鼠要创建一个小鼠模型.带有GNPTAB突变的小鼠在发声过程中有长时间的停顿,这与具有相同突变的人相似。和口吃的人一样,这些老鼠在其他方面都是正常的,这加强了早期的研究,即老鼠可以作为这种障碍的重要特征的有效动物模型。
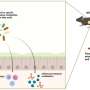
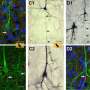
研究人员接着检查了老鼠的脑组织,发现与没有基因突变的老鼠相比,有基因突变的老鼠的星形胶质细胞减少了,但其他类型的细胞没有减少。星形胶质细胞在支持神经细胞方面起着至关重要的作用,它执行着广泛的功能,如供给神经细胞提供氧气和营养,并提供结构支持。
突变小鼠胼胝体中星形胶质细胞的丢失更为明显。此外,使用先进的磁共振成像(MRI)方法,研究人员检测到突变小鼠的胼胝体局部体积减小,尽管MRI值正常,这进一步支持了该大脑区域的缺陷。
它含有多达两亿根神经纤维胼胝体促进大脑左右半球之间的交流,帮助整合涉及两个半球的过程的信号,如身体协调和语言使用。
后续实验中,将GNPTAB人类口吃突变引入个体大脑细胞类型——而不是整个老鼠——证实了发声缺陷是星形胶质细胞特有的。当突变基因被植入到其他类型的脑细胞中时,这些老鼠并没有口吃般的发声。
所有在过去十年中被确认的口吃基因都与细胞内运输有关,细胞利用这个过程将蛋白质和其他成分转移到细胞内的正确位置。细胞运输的缺陷与其他神经疾病有关,如肌萎缩性侧索硬化症(ALS)、帕金森氏症和阿尔茨海默氏症,这表明某些神经细胞通路对这一过程的损伤特别敏感。然而,这项研究并没有表明,持续性口吃是这些其他障碍的早期指标。
如果未来的研究证实,有GNPTAB突变的人的口吃源于大脑中星形胶质细胞的损失,这些发现可能为一些持久性发展性口吃患者打开新的治疗策略的大门,通过靶向相关的分子通路和细胞。
进一步探索