组织模型揭示血脑屏障在阿尔茨海默氏症中的作用
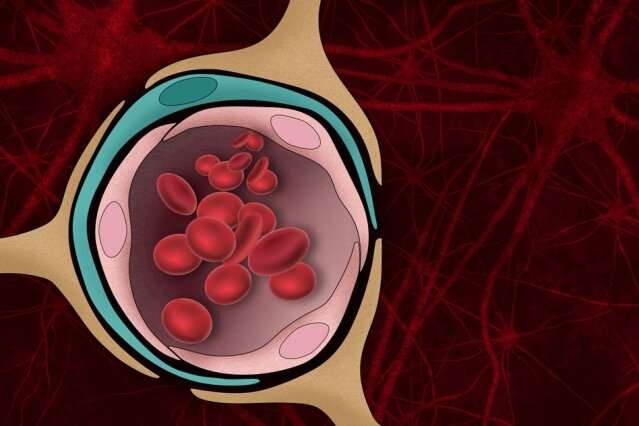
β-淀粉样蛋白斑块,蛋白质聚集在阿尔茨海默氏症患者的大脑中,破坏了许多脑功能,可以杀死神经元。它们还可以损害血脑屏障 - 常紧的边界,可防止血液中有害分子进入大脑。
麻省理工学院的工程师们现在已经开发出一种组织模型,可以模拟β -淀粉样蛋白对血液的影响大脑该研究表明,这种损伤会导致凝血酶(一种通常在血液中发现的凝血因子)等分子进入大脑,对阿尔茨海默氏症的神经元造成额外的损伤。
“我们能够在这种模型中清楚地表明,阿尔茨海默病细胞分泌的淀粉样蛋白β实际上可以损害障碍功能,一旦损害,因子被分泌到脑组织这可能会对神经元健康产生不利影响,”麻省理工学院机械和生物工程的塞西尔和艾达格林杰出教授罗杰·卡姆说。
研究人员还利用组织模型表明,一种可以恢复血脑屏障的药物可以减缓阿尔茨海默氏症神经元的细胞死亡。
Kamm和Rudolph Tanzi是哈佛医学院和马萨诸塞州总医院的神经学教授,他们是发表在杂志上的这项研究的资深作者先进的科学。MIT博士后yojin Shin是这篇论文的主要作者。
屏障破裂
这血管细胞构成血脑屏障的许多专用蛋白质,帮助它们形成紧密的连接蜂窝结构,该结构充当细胞之间的强密封。
阿尔茨海默氏症的患者经常对由β-淀粉样蛋白蛋白引起的脑血管造成损害,这是称为脑淀粉样血管病(CAA)的效果。据信,这种损伤允许有害分子更容易进入大脑。KAMM决定研究这种现象,并通过在微流体芯片上建模脑和血管组织来研究这种现象,其在阿尔茨海默氏症中的作用。
卡姆说:“我们从一开始就试图建立一个模型,用来理解阿尔茨海默病的神经元和脑血管系统之间的相互作用。”“鉴于在研发有效治疗阿尔茨海默氏症的药物方面几乎没有什么成功,过去几年来人们对CAA的关注有所增加。”
他的实验室几年前就开始研究这个项目,与MGH的研究人员一起,他们设计了神经元,使其产生大量β -淀粉样蛋白,就像阿尔茨海默氏症患者的脑细胞一样。
在Shin的领导下,研究人员设计了一种在微流体通道中培养这些细胞的方法,在那里它们产生和分泌β -淀粉样蛋白。在同一块芯片上的一个平行通道中,研究人员培养了大脑内皮细胞,这是形成血脑屏障的细胞。每一种组织类型发育时,两个通道之间都有一个空通道隔开。
细胞生长10天后,研究人员在分隔两种组织类型的中央通道中加入胶原蛋白,使分子从一个通道扩散到另一个通道。他们发现,在3到6天内,神经元分泌的β -淀粉样蛋白开始在内皮组织中积累,导致细胞变得更渗漏。这些细胞还表现出形成紧密结的蛋白质的下降,以及分解通常包围的细胞外基质并支持血管的酶的增加。
由于血脑屏障的破坏,凝血酶能够通过流经有漏洞的血管的血液进入阿尔茨海默氏症的神经元。凝血酶水平过高会损害神经元并导致细胞死亡。
卡姆说:“我们能够证明这种细胞类型之间的双向信号,并真正巩固以前在动物实验中看到的东西,但在一个模型系统中复制它们,我们可以以更多的细节和更好的保真度控制它们。”
堵塞漏洞
然后,研究人员决定试验两种药物,以前已经显示出凝固的内皮组织更简单模型中的血脑屏障。这两种药物都是FDA批准治疗其他条件。研究人员发现,这些药物中的一种,依托枯甲酸,效果非常好,而另一个替代塞米松对其组织模型的泄漏影响不大。
在组织用依托度酸治疗后,血脑屏障变得更紧,而且神经元存活率提高了。麻省理工学院和MGH团队现在正与一个药物发现联盟合作,寻找其他药物,可能能够恢复血脑屏障在老年痴呆症患者。
“我们开始使用这个平台来筛选出于非常简单的单个单元格屏幕的药物,我们现在需要在更复杂的系统中验证,”Kamm说。“这种方法可以提供新的阿尔茨海默治疗潜在形式,特别是因为已经证明了很少的治疗方法是有效的。”
进一步探索












用户评论