SOX9在Alagille综合征中重塑胆汁树
Alagille综合症是一种罕见的小儿遗传症,可影响肝脏,心脏,肾脏,血管,骨架和其他组织。这种情况的一个主要特征是随身携带胆汁的管道中的异常,一种有助于消化脂肪的黄液,从肝脏到胆囊和小肠。Alagille综合征患者的胆管的数量严重降低,这减少了胆汁的正常流动,一种称为胆汁淤积的病症。结果,胆汁在肝脏中产生,导致疤痕可防止肝脏正常工作以执行其代谢功能并消除血液中的废物。
阿拉格尔并发症状是贝勒医学院分子和人类遗传学副教授Hamed Jafar-Nejad的实验室的利益之一。
“即使在同一家庭内,这种疾病的严重程度也在受影响的人群中变化,”Jafar-Nejad解释道。“例如,一些儿童胆汁淤积患者需要一个肝脏移植而另一些则会在小学年龄时表现出显著的改善,从而消除了移植的必要性。“调节这种变化的因素还不清楚。在这项研究中,贾法尔-内贾德和他的同事们发现了新的基因线索,有助于我们理解人类的极端变异
童年的表现肝疾病也为这种情况提供了潜在的治疗途径。
发现的道路
Alagille综合征的大多数病例都是由于JAG1基因缺失造成的,该基因产生jagged 1蛋白(JAG1), jagged 1蛋白是Notch信号通路的重要组成部分。Notch通路参与了细胞间的交流胚胎发育和成人组织维护。来自凹口途径的信号影响细胞如何在显影胚胎中构建体结构。因此,JAG1或NOVCH途径的其他组分的突变导致影响胆管和其他器官的发育过程中的误差。
几年前,Jafar-Nejad实验室为Alagille综合征肝病建立了遗传学代表性的小鼠模型。在该模型中,丢失了一份JAG1(JAG1 +/-)的副本,导致胆汁管道发育受损和后续胆汁淤积。
在目前的研究中,研究小组使用这个模型来识别肝脏疾病的遗传修饰因子,以解释其变异,并确定一个潜在的治疗靶点。研究人员发现,转录因子SOX9的表达水平广泛地改变了小鼠阿拉吉尔综合征肝脏疾病的严重程度。
根据以前的工作,正常小鼠肝脏的完全丧失SOX9基因对胆管开发只有暂时的影响,没有长期后果。在目前的研究中,研究人员发现,在Alagille综合征小鼠(JAG1 +/-)的肝脏肝脏中改变SOX9基因表达,深受影响肝脏病理学。
“看看Jag1 +/-小鼠对SOX9水平有多敏感,令人惊讶的是,SOX9的水平有多敏感,”第一个作者Joshua Adams,AND./PH.D。贝勒的发展生物学计划中的学生。“即使在我们的Alagille综合征小鼠模型中只有一份SOX9基因副本的损失也显着恶化了肝病,显示出增强炎症和肝纤维化的证据。”
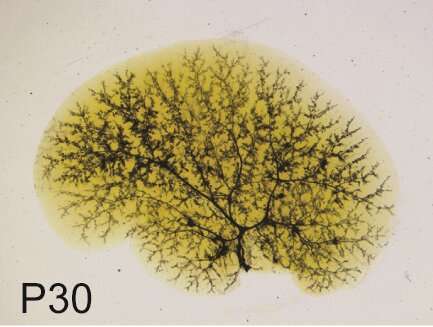
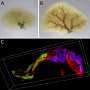
此外,研究人员与辛辛那提儿童医院医疗中心的史黛西·于佩尔博士的团队合作,研究了胆管的结构。1月龄Jag1+/-动物胆总管墨汁注射可见胆树三维结构缺损,但此及其他Jag1+/-肝脏特征随年龄增长而改善。另一方面,同时缺乏一个Jag1基因拷贝(Jag+/-)和一个Sox9基因拷贝的动物在一个月大时情况更严重,而且随着年龄的增长,它们的肝脏状况没有改善。在Jag1+/-动物肝脏中去除Sox9基因的两个拷贝,导致3周龄时的死亡率达到50%,进一步强调了Sox9在Jag1+/-肝脏疾病严重程度中的关键作用。
“我们的数据表明,在Jag1+/-动物中,一个基因(Sox9)的表达水平的改变,可以在人类患者中观察到的肝脏疾病表现中产生全方位的变化,从那些早期胆汁淤积症患者到后来表现出显著改善,一直到需要在相对年轻时进行肝脏移植的患者。”贾法尔-内贾德说。
当贾法尔-内贾德、亚当斯和他们的同事研究阿拉格尔综合征患者的肝脏样本时,他们发现了SOX9可能也与在人类条件下观察到的可变性有关的证据。他们发现,与严重肝病的Alagille综合征患者相比,轻度肝病的Alagille综合征患者肝脏中SOX9的表达水平和模式有很大不同。
SOX9可能是Alagille综合征中的治疗靶标
发现降低SOX9水平的发现增加了Alagille综合征小鼠模型中肝脏状况的严重程度LED研究人员对该模型中增加了SOX9水平可能改善肝脏状况的可能性。
“令人兴奋的是,在Alagille综合征小鼠的肝脏中,Sox9水平的增加大大改善了胆道发育,而不会导致肿瘤的形成,甚至在一年后,”Adams说。“通过进一步了解为什么jag1缺乏的肝脏对Sox9如此敏感,以及Sox9基因表达的增加如何改善胆道发育而不对肝脏产生负面影响,我们可以进一步开发一种治疗Alagille综合征肝脏疾病的策略。”
进一步探索










用户评论