涉及1型糖尿病患者涉及的β细胞的机制揭示

研究人员Lorenzo Pasquali和Mireia Ramos-Rodríguez最近发表于此自然遗传学对引起胰腺β细胞死亡引起炎症反应的机制的研究结果导致1型糖尿病(T1D)的发作。Pasquali是Josep Carreras Leukemia研究所(IJC)的Ramon Y Cajal研究员,Ciberdem隶属于Ciberdem和德国人Trias I Pujol研究所(IGTP),在那里他领导内分泌监管基因组学组。本文第一作者Mireia Ramos-Rodríguez是内分泌监管基因组学组的博士生。该研究与Ulb(Brussels,比利时)的DecíoEizirik合作进行。
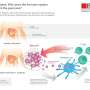
在T1D中,免疫系统有选择地破坏胰腺β细胞,剥夺这种器官生产胰岛素的能力,从而控制血糖。在寻找为什么有些人开发T1D的原因中,研究人员在基因组上鉴定了60多个地区,其中有遗传变异与开发T1D的风险较高,但它们的功能尚未知道。另外,大多数这些变体位于不编码蛋白质并被驳回为“垃圾DNA”的DNA序列中。
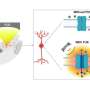
对胰腺的免疫发作细胞由T和B细胞,免疫系统细胞策划。这些细胞渗透了胰岛素在β细胞生活的情况下,通过释放细胞因子和趋化因子,用胰岛素产生的β细胞进行“对话”。在这种“对话”中有些误解是最终导致β细胞失去职能和死亡。为了测试疾病初始阶段的基础,该组分析了变化基因表达,蛋白质生产和DNA结构在β细胞暴露于炎性细胞因子。
只有约2%的基因组含有对应的序列基因这将转化为重要的蛋白质。相反,未被认为没有基因代码的DNA的大量较大部分没有功能。科学家们越来越多地发现这些区域是显着和富含的调节序列,其充当“切换”和控制哪个基因被打开和关闭。
该组发现暴露于炎性细胞因子的暴露会改变β细胞中基因的调节,并影响其功能。它们在胰岛中激活的非编码DNA中映射了大约3,600个区域。他们还观察到暴露于炎性细胞因子诱导DNA折叠的变化,从而使这些非编码区域与其靶基因接触。结果,千种基因被接通并翻译成蛋白质。
该团队发现,在这些基因组的这些新映射的区域中发生了与发育T1D的风险增加相关的遗传变异。“这种调节因子中的DNA变体可能影响胰岛素的细胞对炎症环境的反应的能力,”Pasquali博士说,“这一知识使我们能够了解特定DNA变体促进1型糖尿病的详细机制,“他补充道。
Pasquali的集团使用了一个特别兴趣的模型,因为它模仿胰岛细胞可能在T1D的早期阶段经历的条件。大部分T1D遗传风险显示出影响免疫细胞,在疾病的发展中实施其作用。胰岛细胞本身已被证明具有控制响应危险信号和先天免疫系统的关键步骤的基因。然而,将胰岛基因调节链接到T1D风险的风险没有显着的结果,直到现在。该新数据打开门以揭示作用于胰腺细胞中的分子机制。
现在,该组已经绘制了激活响应胰岛素中炎症环境的基因的开关,测试不同假设的常见遗传变异如何影响T1D中的胰岛细胞。未来的工作可以看出不同的方式免疫系统例如,在疾病的后期阶段强调β细胞。
“这些结果可能适用于其他疾病,”Mireia Ramos-Rodríguez说。“在许多情况下,我们不明白为什么免疫细胞攻击某种细胞类型。疾病相关刺激中的监管元素的解剖使我们更接近理解的不仅是T1D,还具有其他自身免疫性疾病。”
进一步探索













用户评论