朊病毒蛋白丛如何?也许可以解释DNA-modulated液体滴
里约热内卢联邦大学的研究人员(UFRJ),在巴西,已经确定,朊病毒蛋白质和DNA之间的相互作用可能是背后的形成蛋白质淀粉样蛋白聚集和克雅二氏症等神经退行性疾病的出现和其他海绵状脑病。这项研究发表在今天的美国实验生物学学会联合会杂志。
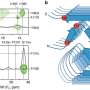
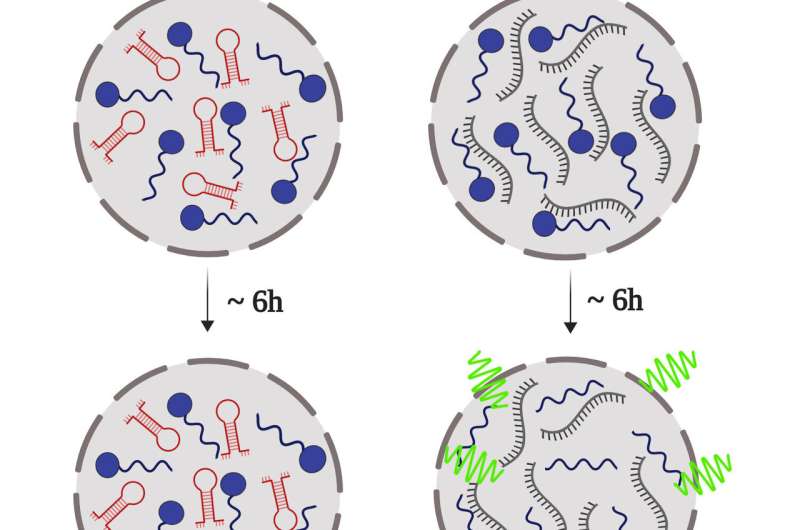
由UFRJ教授Yraima Cordeiro ibsen Pinheiro和安德森,科学家们已经发现,朊蛋白(PrP)遭受液-液分离阶段,这种机制是精细控制的一些DNA序列。在一个类似的过程油滴在油水乳液分散,DNA导致PrP形成的液滴,把它变成胶状甚至改变成固体。他们还注意到,这些属性依赖于DNA适体的构象(发夹或延长构象)和化学计量学的protein-nucleic酸的相互作用。
把液体滴变成的过程固态可以解释异常的形成和不可逆转的朊蛋白的聚集,称为淀粉样蛋白聚集。这些结构都是有毒物质,对大脑和相关传染性海绵状脑病的发展,如克雅二氏症和牛海绵状脑病(BSE),俗称疯牛病。淀粉样蛋白聚集和疾病之间的联系已经很多年了,但是这些结构形式仍不清楚。研究带来的见解,可能有助于回答这个问题。
研究的主要发现启发的财产朊蛋白以类似的方式结合核酸蛋白质可以导致其他神经退行性疾病。这将打开的可能性,针对疾病通过选择特定的DNA序列来控制或避免细胞器变成非功能性凝胶和固体。
进一步探索