使用精密外观蛋白酶编辑的小鼠固定遗传脑障碍
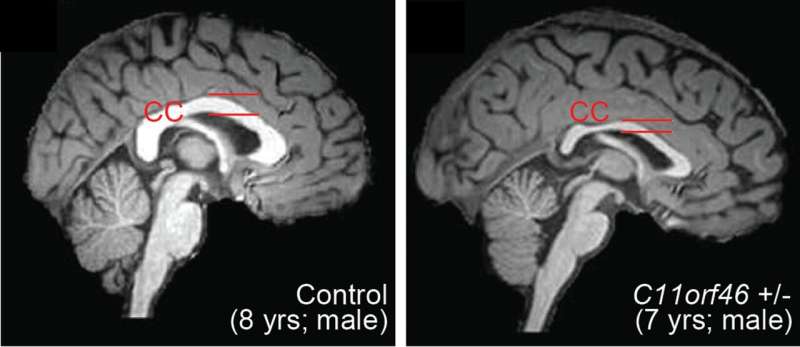
在培养的小鼠脑中使用靶向基因外观蛋白酶编辑方法,约翰霍普金斯医学研究人员逆转了一种基因突变,导致遗传障碍WAGR综合征,这导致人们的智力残疾和肥胖。这种特定的编辑是独一无二的,因为它改变了外观内血珠 - 基因的调节方式 - 而不改变受调节基因的实际遗传密码。
研究人员发现,这个名为C11orf46的基因是一种重要的调控因子大脑发育。具体而言,它转动方向和关闭方向感蛋白质,帮助引导长纤维从负责发送电信的新形成的神经元生长出来,帮助它们形成束的束,这连接了大脑的两个半球。未能正确形成这种捆绑结构,称为胼胝体,可以导致诸如此类的条件智力障碍,自闭症或其他大脑发展障碍。
"Although this work is early, these findings suggest that we may be able to develop future epigenome editing therapies that could help reshape the neural connections in the brain, and perhaps prevent developmental disorders of the brain from occurring," says Atsushi Kamiya, M.D., Ph.D., associate professor of psychiatry and行为科学约翰霍普金斯大学医学院
这项研究在线发表在9月11日出版的《科学》杂志上自然通信。

wwagr综合征又称11p13染色体缺失综合征,当包含C11orf46的11p13染色体区域的部分或全部基因偶然缺失时,可导致wwagr综合征。研究人员使用了一种基因工具,短发夹RNA,以减少小鼠大脑中C11orf46蛋白的生成。C11orf46蛋白含量较少的小鼠大脑神经元纤维不能形成神经元束胼胝体,这与wwagr综合征中发现的情况相同。
具有较低C11orF46的小鼠中,使信号蛋白6a,方向感蛋白质的基因更高。通过使用改进的CRISPR基因组编辑系统,研究人员能够编辑Semaphorin的基因的一部分调节区域。这种EngeaGenome的编辑允许C11ORF46结合并折起这些小鼠的大脑中的基因,然后将神经元纤维捆绑恢复到正常脑中的内部发现。
进一步探索















用户评论