过度活跃的Foxa1重新编程内分泌抗性乳腺癌变成转移性
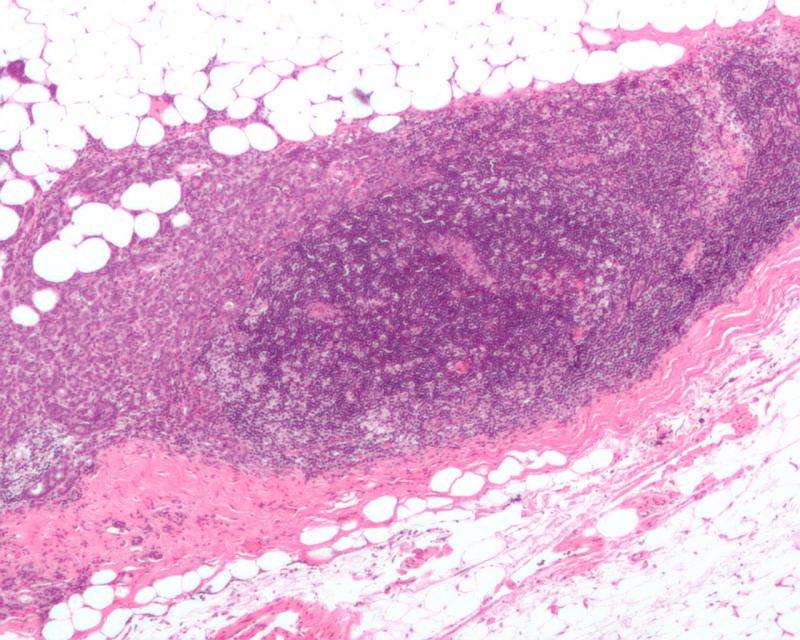
由贝勒医学院和哈佛医学院的研究人员领导的团队推出了一种新的机制,有助于解释内分泌抗性乳腺癌如何获得转移性行为,打开新的治疗策略的可能性。
发表在这件事中国家科学院的诉讼程序,该研究表明,过度活跃的FOXA1信号传导,其先前在内分泌抗性转移中报道乳腺癌,触发基因组重新编程,导致耐治疗和转移行为的抵抗力。
研究人员还将HIF-2A鉴定为FOXA1的重新编程的关键介体,并显示目前HIF-2A的抑制剂临床开发用于治疗先进的肾细胞癌和复发性胶质母细胞瘤,可以有效地减少内分泌抗性的迁移和侵袭胸部癌细胞表达高Foxa1活动。
“约75%的乳腺癌具有雌激素受体,因此它们被称为雌激素受体正(ER +)。原始ER +乳腺癌细胞依赖于雌激素生长,并且使雌激素与细胞不可用的疗法,称为激素疗法,可以导致一些患者的长期缓解。Tamoxifen是几种类型的激素治疗之一,通过结合并阻断癌细胞上的雌激素受体,“贝勒副教授瑞秋席克林副教授瑞秋·席克副教授(Baylor)。
然而,大多数患有转移性疾病的患者,包括肿瘤最初反应的那些肿瘤治疗,最终因肿瘤的抗激素治疗抗性而最终复发和死亡。
在以前的工作中,Schiff和她的同事发现,抗激素治疗的肿瘤细胞比易感细胞更多的FOXA1,并且这种丰富的FOXA1在赋予治疗抵抗力方面发挥着积极作用。在目前的研究中,研究人员采取了一种基因组的方法来深入挖掘Foxa1如何完成触发转移行为的复杂任务。
“在实验室中使用乳腺癌细胞系,我们发现Foxa1通过打开前面关闭的某些基因并关闭其他基因来重新编程内分泌治疗抗性乳腺癌细胞。新的基因表达程序模拟早期胚胎发育计划赋予癌症细胞具有新的能力,例如能够迁移到其他组织并积极入侵它们,转移行为的标志,“分子和细胞生物学助理教授副通富,部分贝勒的莱斯特和苏史密斯乳房中心。
研究人员还发现Foxa1并没有单独行动。随着其他因素,它激活了大量的增强剂,该增强剂共同地同步基因组电池重新编程。HIF-2A是使用FOXA1的顶部增强剂,介导激活Pro-Metapatic Gene集合和与临床结果不良相关的途径。
重要的是,研究人员在实验室细胞实验中显示,HIF-2a的抑制剂减少了抗迁移和侵蚀内分泌的侵蚀性乳腺癌细胞表达高Foxa1活动。
“与来自哈佛医学院的同事合作,我们探讨了将这些发现转移到诊所的可能性。我们分析了临床转移性乳腺癌数据集,并发现了类似于我们内分泌抗性乳腺癌细胞模型中的重编程事件,“Schiff说,贝勒也是Dan L Duncan综合癌症中心的成员。
在一起,这些发现揭示了富氧化物机制的细节,福克斯1触发器诱发内分泌抗性乳腺癌中的转移行为,其他报告也存在于其他类型的癌症中,例如前列腺和胰腺癌。此外,调查结果还支持进一步探索抑制HIF-2a或其他增强剂,以控制内分泌治疗耐药乳房中许多基因的表达癌症可以转化为有效的治疗策略。














用户评论