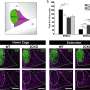
科学家们渴望解释大脑节律增强对阿尔茨海默症模型的广泛影响

在小鼠模型中,大脑中增加40Hz的“伽马”节律功率可以影响阿尔茨海默氏症的病理和症状,这一广泛程度令人惊讶,甚至对率先提出这一想法的麻省理工学院神经科学家来说也是如此。如此令人惊讶,事实上,他们还不能解释为什么会发生这种情况。
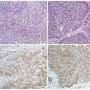
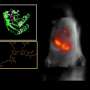
在三篇论文中,包括今年的两篇细胞而且神经元,他们已经证明,将老鼠暴露在40赫兹的灯光闪烁或声音嗡嗡声中,这种方法被称为“GENUS”,即使用感官刺激的伽马诱捕法,加强了整个大脑的节奏,并改变了多种脑细胞类型的基因表达和活动。病理性淀粉样蛋白和tau蛋白的建立下降,神经元及其电路连接受到保护,不变性,学习和记忆的持久性明显优于未接受GENUS的疾病模型小鼠。
在一篇新的评论文章中神经科学的发展趋势领导这项工作的两名研究人员列出了必须了解的少数已知和许多未知,以确定广泛的影响是如何发生的。这是一个他们喜欢的挑战,因为答案既可以打破新的科学基础,也可以帮助他们改进GENUS如何成为一种治疗或预防的方法。
“虽然我们知道它会影响老鼠的病理,但我们想了解它是如何影响的,因为这将帮助我们理解和改进潜在的治疗方法,”该研究的第一作者Chinnakkaruppan Adaikkan说,他是高级作者Li-Huei Tsai的实验室的博士后,Li-Huei Tsai是神经科学的Picower教授和Picower学习与记忆研究所的主任。
Adaikkan从他的博士研究开始就对了解神经活动是如何产生大脑节律感兴趣。在麻省理工学院,他将这种激情引导到理解感官刺激如何引入振荡。
Adaikkan说:“这就是驱使我每天来实验室研究这些机制的原因。”“当我们从第一只老鼠身上得到数据时,我们记录了视觉皮层,海马体和前额叶皮层,我们惊讶地发现视觉刺激在这些大脑区域内。这非常令人兴奋,但要了解这是如何发生的,我们还有很长的路要走。”
这篇新论文提出了这个问题以及该领域的许多其他问题。什么细胞是大脑对GENUS反应的基础?如何γ节律作用于非神经元细胞,如星形胶质细胞和小胶质细胞?它是如何在负责感知的大脑区域之外传播的?增强伽马能在多大程度上影响认知?长期刺激会影响大脑回路连接吗?它们是如何改变的?
细胞的角色
关于神经元群如何参与电活动的相干振荡的研究产生了两种解释伽马节律的模型。Adaikkan和Tsai写道,两者都涉及兴奋性神经元和抑制性神经元之间的相互作用,但在哪种类型主导相互作用方面存在差异。在他的工作中,Adaikkan试图剖析特定神经元类型在GENUS中的作用,以及这些模式与其他伽玛源(如认知任务调用的伽玛)的相似程度。
GENUS影响的不仅仅是神经元。蔡的实验室发现小胶质细胞改变了它们的基因表达它们的物理形态、蛋白质消耗行为和炎症反应取决于所涉及的阿尔茨海默氏症模型。另一个研究小组的研究表明,阻止星形胶质细胞的囊泡释放可以阻碍小鼠的伽马能量。蔡的小组发现,听觉GENUS招募了更多的反应性星形胶质细胞,这些细胞更倾向于消耗病理蛋白。
关于这种“神经胶质”细胞是如何参与其中的,这篇新论文提出了三种假设:它们可能通过调节携带电荷的离子流动,直接参与伽马夹带;即使它们对节律没有贡献,它们的离子敏感性可能仍然使它们对伽马的变化有反应;相反,它们可能受到伽马射线导致的神经递质水平变化的影响。
此外,不同的神经胶质细胞也可能参与其中,因为它们接近称为突触的神经元之间的电耦合,或者因为它们的活动是如何由神经活动控制的。
更广阔的大脑
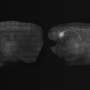
这种GENUS延伸到海马体和前额叶皮层,海马体是记忆的关键,而前额叶皮层是认知的关键,这可能是它如何保持大脑功能的一个因素。但是,对于增加的伽马如何促进多区域通信,仍然存在相互竞争的模型。作者写道,在一个模型中,相同频率的相干性优化了通信,而在另一个模型中,一个区域的伽马活动直接驱动下游区域的活动。他们认为,直接操纵区域间电路的新实验可以帮助确定哪种模型能更好地解释伽玛夹带效应。
最后,GENUS对大脑功能和行为的影响也没有完全解释清楚。蔡氏实验室的实验显示,空间记忆有显著的效果,其他形式的记忆也有一些效果,这取决于刺激方法。其他研究表明,刺激大脑通过其他方式,如通过基因或光基因操纵小鼠的节律,或通过对人类的经颅刺激,也可以改善工作记忆等功能。Adaikkan感兴趣的是缩小这些研究与蔡实验室的工作之间的差距:大多数研究都是在刺激过程中测量认知表现,而蔡实验室是在重复刺激结束后进行的。他说他也想在GENUS积极进行的同时测试老鼠的表现。
蔡说:“我们的实验室很高兴能解决这么多的假设,并看看这个领域如何解决更多的假设。”“GENUS为神经科学创造了许多有趣的新问题。”