凝血蛋白和血小板促进免疫逃避,癌症进展

俄亥俄州立大学综合癌症中心阿瑟·g·詹姆斯癌症医院和理查德·j·索洛夫研究所(OSUCCC-James)的研究人员领导的一项新研究揭示了凝血蛋白和血小板是如何促进癌症进展和抑制对癌症的免疫反应的。
研究结果显示了凝血酶(血液中的一种凝血蛋白)是如何引起的血小板释放转化生长因子- 1 (TGF-b1),这种物质可以促进乳腺癌、前列腺癌、结直肠癌和其他癌症的疾病进展,并抑制免疫系统对前列腺癌的反应癌症.
此外,TGF-b1是癌症患者中诸如PD1抑制剂等免疫疗法失败的主要原因。本研究可能提供一个新的解释是什么原因导致肿瘤抵抗免疫疗法并对治疗药物变得敏感。
研究人员使用动物模型证明,抑制凝血酶活性可以阻止TGF-1b的释放,并使对抗pd -1免疫治疗有耐药性的肿瘤对这些药物敏感。
该研究结果发表在该杂志上科学转化医学.
“在这项研究中,我们描述了凝血酶和TGF-b1之间的直接联系,TGF-b1是一种促进肿瘤首席研究员李子海博士说,他是俄亥俄州立大学肿瘤医学学部的教授,也是OSUCCC-James的Pelotonia免疫肿瘤研究所(PIIO)的创始主任。李还在俄亥俄州立大学医学院担任癌症研究的克鲁兹纪念主席
“我们还表明,系统地干扰这一机制可以阻止TGF-1b的释放,并导致肿瘤微环境的变化,这有利于抗癌免疫反应,”李说,他是OSUCCC-James转化治疗项目的成员。
李指出,癌症类似于未愈合的伤口,不断激活凝血通路,在肿瘤内部和周围产生高浓度的凝血酶。这反过来又会导致慢性血小板激活和TGF-1b的释放。
“TGF在癌症发展中扮演着重要的角色,”Li说。“具体来说,TGF-b1改变了肿瘤微环境,保护癌细胞免受免疫细胞的攻击。”
Li补充说,研究表明抑制TGF-b1可以增强癌症免疫治疗。“如果我们能有效抑制TGF-b1的成熟或功能,它将为癌症治疗开辟新的途径。”
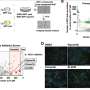
在这项研究中,Li和他的同事使用了来自癌症患者的血液样本、遗传分析、细胞系和动物模型来调查成熟TGF-1b释放的机制,以及阻断其释放作为癌症免疫治疗手段的意义。
主要结论包括:
- 凝血酶裂解一种叫做GARP的分子(主要是糖蛋白a重复),这种分子存在于血小板表面;
- GARP的裂解导致成熟的TGF-1b从血小板中释放;
- 这种裂解是激活血小板TGF-b1所必需的;
- 使用抑制剂达比加群酯阻断凝血酶大大改变肿瘤微环境增加了肿瘤浸润T细胞、自然杀伤细胞和中性粒细胞的数量和活性。
“总的来说,我们的研究揭示了癌症免疫逃避的机制,包括凝血酶介导的GARP裂解和血小板释放TGF-b1,”Li说。“这也表明,阻断GARP的分裂可能是克服癌症对免疫疗法的抵抗的一种有效的治疗策略。”
进一步探索