肠道微生物与胸腺中免疫细胞的新沟通
新生儿在出生后立即面临着独特的免疫挑战。当他们离开相对无菌的胎儿环境时,它们突然暴露于多种外来抗原,其主要负担是微生物群的形式新殖民胃肠道。这些迅速乘以外国入侵者代表,到目前为止对新生儿免疫系统的最大威胁,这必须识别和分类这些生物作为良性,共生或致病性。
研究表明,早期微生物和粘膜之间有效的“串扰”或沟通免疫细胞对健康的微生物社区的形成至关重要,促进功能良好免疫系统。参与粘膜免疫的免疫系统的细胞在叫做胸膜胸部下方的胸腺下的器官中。到目前为止,如果肠道微生物在胸腺中影响这些细胞的发展,则目前尚不清楚早期生活。
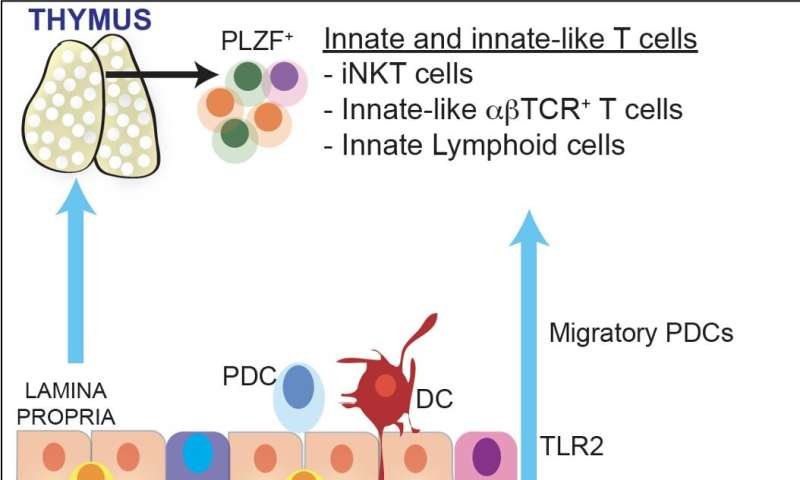
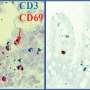
Massachusetts综合医院粘膜和免疫学生物学研究中心(MIBRC)的研究人员现在报告说,肠道微生物调节胸腺中专门的免疫细胞的发展,在粘膜耐受性中发挥着关键作用。他们广泛研究的调查结果已发表于此国家科学院的诉讼程序本星期。NITYA JAIN,PH.D和同事专注于表达转录因子PLZF的免疫细胞的子集。这些细胞,统称称为先天和先天淋巴细胞,通常在肠粘膜屏障界面上起作用,并在粘膜部位提供免疫保护。
研究这些免疫细胞在背景下的发展肠道微生物,研究人员单殖民化无菌小鼠通过模型人类共生,Bragonoides fragilis,并证明了这种单一的细菌可以在婴儿小鼠的胸腺中恢复Plzf +先天和先天淋巴细胞的发育。在进一步的概念证明研究中,他们表明缺乏多糖A(PSA)表达的突变体B.胰蛋白酶不能这样做,表明特定的微生物抗原可以调节这种早期生命的发展过程。在突变小鼠中观察到这些细胞中的类似缺陷,其缺乏受体2的表达,识别细菌和细菌组分,包括B.Fragilis PSA,引发宿主保护免疫反应。
为了了解这种微生物消息如何递送至发展胸腺细胞,Jain的组使用新的小鼠模型来跟踪细胞从结肠迁移到胸腺。在2018年可视化实验期刊的Wellman Centre of Mgh's Guillermo“Gary”Tearney的Groundne of MgHilmo“Gary”Tearne的Guarthery的帮助下发达了光转换策略。
研究人员表明,一类被称为血浆曲线细胞细胞(PDC)的抗原呈递细胞被肠道微生物印象,并在早期生命中从肠道迁移到胸腺中,以调节胸腺淋巴细胞的发育。耆那教说,这是吉恩的集团揭示了“肠道微生物与胸腺中的细胞之间的新沟通”。“它在早期生命中塑造了免疫'曲目',并影响宿主如何在整个寿命期间对疾病作出反应。”
婴儿的不平衡发展肠道微生物组被认为在稍后在生活中发挥作用。例如,通过抗生素或饮食扰乱婴儿婴儿的微生物群,与患有乳糜泻和炎症性肠病(IBD)的过敏性,哮喘和自身免疫疾病的风险增加。Jain的集团展示了这种观察的机制基础。他们表明胸腺PLZF +细胞在早期使用广谱抗生素治疗的小鼠中没有有效地发展,但在后期生命中处理的小鼠被施加。
Jain说,当在胸腺中的免疫细胞在胸腺中尤其易受微生物影响时,“似乎是早期生命时间窗口。”此外,该研究表明,微生物诱导的脑脂生先生先天和先天性细胞的改变的脑脂发生的改变持续存在于成年期,并导致对实验性结肠炎的敏感性增加。重要的是,通过PLZF +的转移可以使疾病严重程度进行调节细胞Jain说,来自常规微生物群的小鼠,jain说。她补充说,“这对治疗IBD等自身免疫性疾病的策略设计具有重大影响。我们的研究指出了以前可以作为患者的养殖细胞疗法发展的先前未开发的途径。”
MIBRC主任Alessio Fasano,MD指出,日益增长的证据表明,健康免疫国家的早期发展需要发育婴儿及其微生物群落之间的理想共生关系。“我们如何选择”我们的理想微生物队教导我们的免疫系统来捍卫我们而不是伤害我们仍然是一个大问号。尼尼达和她的团队 - 第一次 - 第一次对负责的早期机制的揭示法丹诺说,建立人体宿主和微生物组之间的健康关系。
进一步探索









用户评论