胃疾病的分子开关
传染病引发的细菌和其他微生物是人类最常见的原因在全球死亡率。大约一半的世界人口携带stomach-infecting细菌幽门螺杆菌(幽门螺旋杆菌),这是最重要的危险因素溃疡、麦芽胃淋巴瘤和腺癌。快速传播的病原体对抗生素产生抗药性,使它越来越难治疗这些感染使用抗生素治疗。一个研究小组从Friedrich-Alexander-Universitat埃(能力)已经公布了新的机制,控制感染幽门螺杆菌的原因。这些发现可能最终导致新疗法。该研究发表在《华尔街日报》自然通讯。
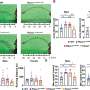
团队领导的国家和国际科学家史蒂芬博士教授Backert从椅子上微生物的能力调查细菌如何操纵宿主的免疫系统,以确保其长期生存的胃。一个慢性炎症是最常见的胃疾病诸如此类的原因。研究人员发现了一种分子开关,使用一个前所未知的机制来调节炎症反应在胃里。
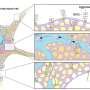
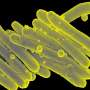
幽门螺杆菌和胃细胞之间的交互激活一个注射器一般的纤毛结构称为IV型分泌系统。CagL,蛋白质是在这个结构的表面,允许细菌毒素CagA蛋白质被交在胃癌细胞。然后注入CagA re-programs宿主细胞胃癌可以开发。现在看来,CagL还有另一个重要功能,然而。免疫系统识别的蛋白质是通过受体TLR5。小鼠模型实验表明,TLR5控制感染有效。CagL模仿TLR5识别主题在其他病原体的鞭毛蛋白的蛋白质,从而控制人类的免疫反应。
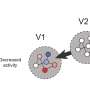
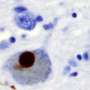
有趣的是,这信号通路可以打开和关闭的IV型分泌系统,不被认为是与其他细菌。据推测,幽门螺杆菌已经利用这种信号通路在几千年的进化,消除“麻烦”细菌竞争对手在胃里。与此同时,CagL先天和适应性的影响免疫系统以及炎症反应,幽门螺旋杆菌本身并不认可,因此不能消除了机制至关重要的长期在胃和幽门螺杆菌感染引发胃病。研究人员还发现,TLR5不再是健康的胃细胞中产生,或胃细胞感染后解决。这表明这种蛋白质的表达是一种新的指标胃病在人类由幽门螺旋杆菌引起的。
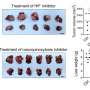
Backert教授希望这些发现能帮助开发重要的抗菌治疗新方法,作为CagL, CagA和TLR5很好治疗。参与研究人员已经开始测试合适的物质。“我们希望特定抑制剂可以麻痹IV型分泌系统的功能或部分或完全避免感染Backert教授,”报告。
进一步探索