与卵巢癌相关的蛋白质会加剧阿尔茨海默氏症的神经退行性变
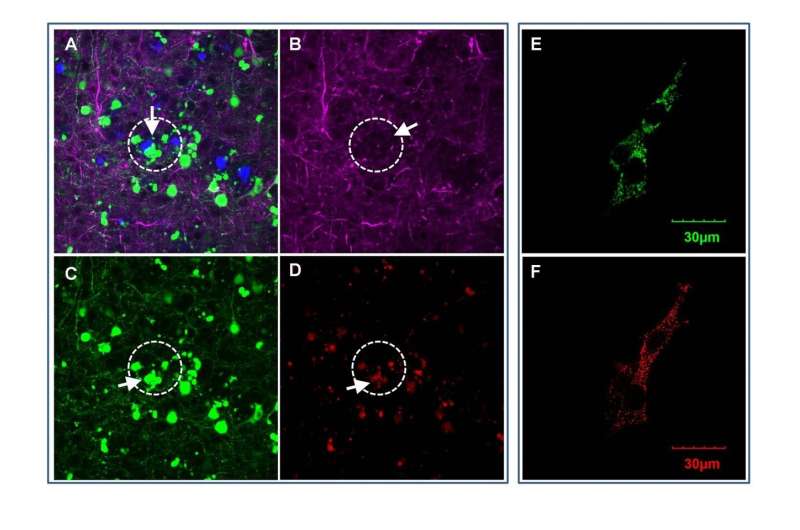
休斯顿卫理公会的科学家们通过结合计算方法和实验室研究,发现了一种在卵巢癌中发现的蛋白质,这种蛋白质可能会导致大脑功能下降和阿尔茨海默病。
休斯顿卫理公会癌症中心生物信息学和生物统计中心副主任Stephen T.C. Wong博士说:“我们的发现表明,另一种已知的蛋白质可能在这里发挥作用,这可能有助于我们有朝一日确定新的治疗靶点。”“这些发现可能表明这种蛋白质有不同的作用β淀粉样蛋白在神经退化。许多阿尔茨海默氏症研究人员一直关注淀粉样蛋白或者β淀粉样蛋白和另一种蛋白质tau之间的联系。”
在该杂志在线发表的一项研究中EBiomedicine, Wong和他在休斯顿卫理公会医院Ting Tsung and Wei Fong Chao BRAIN中心的团队,报道了OCIAD1(卵巢癌免疫反应抗原结构域含1)的新作用卵巢癌在转移和干细胞代谢方面,Wong的小组在人类中发现了OCIAD1蛋白大脑并确定它会损害大脑中的神经元和突触,导致阿尔茨海默病的神经退行性变。
“我们的研究解决了阿尔茨海默病的一个基本问题——如何或是否可以在20年前看到β淀粉样蛋白的积累大脑功能退化涉及进行性神经退行性疾病,”王说,他是约翰·S·邓恩(John S Dunn Sr.)的杰出主席生物医学工程休斯顿卫理公会医院肿瘤学计算机科学和生物工程教授。“研究导致阿尔茨海默氏症患者病情逐渐下降的因素将有助于我们开发诊断性生物标志物和新的治疗方法。”
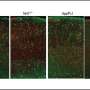
科学家们筛选了已故阿尔茨海默病患者脑组织的生物信息学存档数据,以及混合的小鼠模型计算方法实验室研究。他们确定OCIAD1通过损害线粒体功能在疾病的进行性神经退行性变中发挥作用。线粒体被称为细胞的发电站,对线粒体的损伤会导致大脑中细胞死亡的涓滴效应,从而导致神经元损伤。
“我们应用了系统生物学策略,看看我们是否能找到阿尔茨海默病神经退行性变的不同机制。我们确定了OCIAD1作为一种新的神经退行性变相关因子,预测了它的功能,并证明了它通过损害线粒体功能介导β淀粉样蛋白对细胞和突触损伤的长期影响,”李旭平博士说,他是黄的团队的共同通讯作者和讲师。
阿尔茨海默病的研究传统上集中在几个主要的主题上——淀粉样蛋白在神经元损失中的作用以及它是如何有毒的蛋白质与tau蛋白相互作用导致损伤。然而,最近,其他研究认为β淀粉样蛋白只是一个旁观者,并质疑它是否会导致神经元变性。
Wong的小组接下来打算研究OCIAD1是否在阿尔茨海默氏症淀粉样蛋白β和tau聚集物的两种已知变化之间的相互作用中发挥作用。如果是这样,更多的研究将集中在OCIAD1作为生物标志物或治疗靶点的潜力上。
阿尔茨海默氏症影响着超过580万美国人,随着老龄化人口寿命的延长,这种疾病的流行程度预计将会增加。根据阿尔茨海默病协会和疾病控制与预防中心的数据,阿尔茨海默病是美国最昂贵的疾病,2019年估计花费2900亿美元。
更多信息:李旭平等,OCIAD1通过诱导线粒体功能障碍、神经元脆弱和突触损伤参与阿尔茨海默病的神经退行性变,EBioMedicine(2020)。DOI: 10.1016 / j.ebiom.2019.11.030