干细胞、CRISPR和基因测序技术是新的脑癌模型的基础

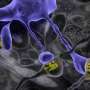
加州大学圣地亚哥分校医学院的研究人员利用基因工程的人类多能干细胞创造了一种新的癌症模型进行研究在活的有机体内胶质母细胞瘤,最常见和侵袭性的脑癌,如何发展和变化的时间。
共同高级作者Frank B. Funari博士说:“我们已经开发了经过crispr工程设计的干细胞模型,在胶质母细胞瘤中具有与肿瘤相关的驱动突变,这基本上包含了患者来源肿瘤的所有特征,包括染色体外DNA扩增。”他是加州大学圣地亚哥分校医学院病理学系的教授,也是路德维希癌症研究所圣地亚哥分校肿瘤生物学实验室的负责人。
“这些模型,或者我们称之为阿凡达,使我们能够长期研究人类肿瘤的发展在活的有机体内,这对于病人来源是不可行的组织样本它已经包含了其他的基因变化。”
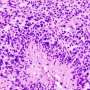
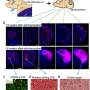
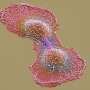
报道于2020年1月28日自然通讯在美国,研究人员利用CRISPR编辑技术,让原本“正常”的基因组发生精确突变,从而创造出促进肿瘤发展的遗传条件。由此产生的化身是惟一的,它们像一个4级glioma-a快速增长类型的肿瘤开始在大脑的神经胶质细胞的病理学、转录组签名,设计基因突变的基因改变和演化,如染色体外的DNA和染色体重组的出现。
“单细胞RNA测序和计算工具的加入使得对大数据的高效分析成为可能,从而真正评估我们的化身中惊人的肿瘤内异质性,这复制了在患者样本中看到的东西,”共同高级作者Gene W. Yeo博士说。他是加州大学圣地亚哥分校细胞与分子医学系和基因组医学研究所的教授,也是桑福德再生医学联盟的成员。
现有的小鼠模型用于测试药物的特定突变,但没有考虑到肿瘤发展的多种途径。人体组织样本不允许标准化测试。作者说,这种新的化身建模系统为肿瘤生物学和进化的标准化研究提供了一个平台。
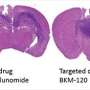
Yeo说:“我们现在可以测试癌症基因组计划预测的哪些突变是真正的肿瘤驱动因子,以及它们如何变得具有侵袭性。”“更重要的是,这些癌症化身为药物发现提供了系统性、可控的机会。”
胶质母细胞瘤是高度恶性的。标准的治疗是积极的:手术,然后是化疗和放疗。然而,大多数肿瘤在六个月内复发。两年的存活率是30%。
这种化身模拟了在人体内观察到的肿瘤内异质性,使其成为详细检查的一个很好的选择肿瘤Furnari说,进化和寻找基于驱动基因的治疗弱点。
Furnari说:“接下来的步骤包括筛选药物,测试成人和儿童脑肿瘤的其他突变,以及评估这些方法是否可以模拟胰腺和肺部等其他组织的肿瘤。”
进一步探索










用户评论