als神秘由蓝色光照亮
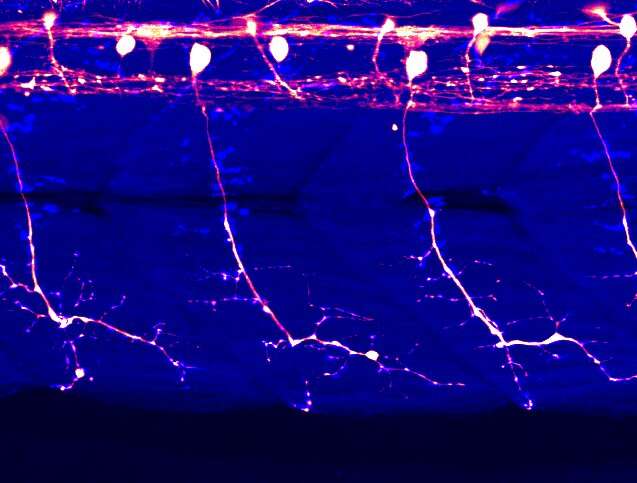
日本联合研究组通过使用光照照明远程控制疾病相关的蛋白质分子通过远程控制疾病相关的蛋白质分子而成功地在小型热带鱼中再现了关键的ALS症状。
在肌营养的外侧硬化(als),也称为lou gehrig的疾病或运动神经元疾病,神经细胞称为运动神经元逐渐退化。这些电动机神经元累积含有TDP-43蛋白的聚集形式的夹杂物。
在人体,运动神经元沿着脊髓的长度排列,并沿着称为轴突的电缆延伸,与覆盖体表的肌肉相连。这种解剖特征使运动神经元成为最难以观察的细胞之一。因此,我们不完全了解在肌萎缩性侧索硬化症中,健康的运动神经元何时以及如何开始变得异常和病态。
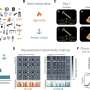
在上周在期刊发布的一项研究中自然通信通过将人类TDP-43附着在一种植物蛋白上,这种植物蛋白在吸收蓝色时会形成蛋白质聚集体,从而设计出一种新的TDP-43变体光。这种受光控制或“光遗传”的TDP-43在黑暗中正常发挥TDP-43的功能,但在蓝光照射下逐渐形成聚集体。作者将重点放在斑马鱼的运动神经元上,因为它们与人类的运动神经元有几个共同的特征。由于鱼体是透明的,所以可以看到整个细胞(图)。利用他们独创的技术,作者在斑马鱼运动神经元中表达了光遗传TDP-43,并发现当鱼仅仅被蓝光照射时,ALS的关键病理就出现了(电影)。
出乎意料的是,即使在透光效力和聚阳素TDP-43聚集之前,电动机神经元和肌肉之间的连接也会削弱。这结果表明电机神经元在TDP-43发展成在ALS末期观察到的典型的大聚集体之前就已经被破坏了。
领导这项研究的浅川博士说:“这项研究首次表明,TDP-43聚集是导致这种疾病的原因发动机动物的神经元功能障碍。我们认为,称为TDP-43低聚物的小TDP-43组件可能会对运动神经元比更大的集合。”
他继续说:“我们现在可以通过控制光照强度和照明位置,以临时和空间调整的方式产生一种类似als的状态。未来几年,我们的最终目标是找到能够防止光遗传TDP-43形成低聚物和聚集体的化学物质,我们希望这些化学物质能够用于ALS治疗。”
进一步探索














用户评论