人体肠道式模型有助于定义“泄漏的肠道”,并概述治疗途径
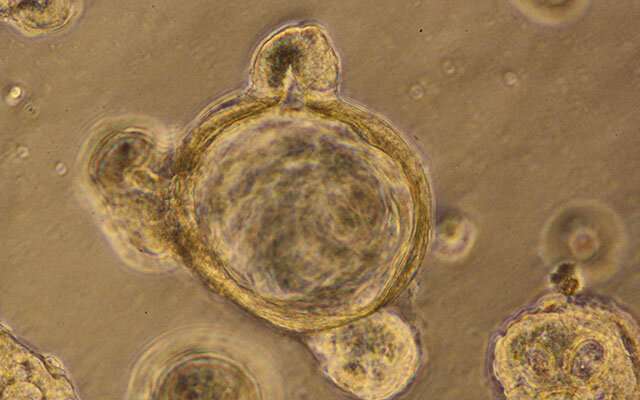
曾经是各种疾病的模糊替罪羊,越来越多的证据表明,一种被称为“肠漏”的情况——微生物和其他分子从肠道中渗出——可能比以前认为的更常见,更有害。
肠漏最常发生在老年人、癌症患者或其他慢性病患者,以及生活压力特别大的人身上。压力会破坏细胞这种形式的肠衬。随后通过这些细胞间隙泄漏的微生物和分子可以触发免疫反应,导致由慢性炎症, 如炎症性肠病,痴呆,动脉粥样硬化,肝纤维化,癌症,糖尿病和关节炎。
然而,临床医生告诉谁拥有谁肠漏谁不是呢?而且没有治疗方法。
加州大学圣地亚哥分校医学院的研究人员现在第一次能够模拟肠道渗漏的情况,使用病人细胞生成的人体肠道三维模型。这些小型类器官,或“迷你内脏”,揭示了新的生物标志物,帮助定义什么是漏肠-分子信号这将有助于临床医生更好地诊断病情,跟踪病情进展,评估治疗的成败。该团队还使用该模型来探索一种潜力途径用一种常见的、可用的药物来收紧渗漏的肠道。
该研究于2020年2月10日发表于生命科学联盟该研究由第一作者prapta Ghosh医学博士(加州大学圣地亚哥分校医学院和摩尔斯癌症中心细胞和分子医学教授)和资深作者Soumita Das博士(加州大学圣地亚哥分校医学院病理学副教授)领导。
高希和他的同事发现了之前确认这是一种特殊的分子机制,有助于收紧肠道粘膜连接,他们将这种机制称为压力极性信号通路。他们发现,当通路受到压力时,连接点会消失。他们还发现,糖尿病药物二甲双胍可能有助于激活该通路,收紧连接。但这些基本的发现是在培养皿中培养的细胞系中发现的,与人类无关——至少目前还没有。
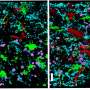
所以纪念,DAS和团队转向了人类测试主题的下一件最好的事情:3-D肠细胞器来自患者的肠道。肠道的衬里并不顺利,但更多类似于粗糙的地形,有许多山峰和山谷。在每个山谷的底部,被称为隐窝,活小储存器的干细胞。为了生产肠器有机体,研究人员从患者活组织检查中收集了微量的这些干细胞,并在实验室中赢得了它们。当他们在一个人的肠道中,干细胞分化为或专业化到构成肠衬的四种不同的细胞类型中。但在实验室里,他们在身体外面,他们卷成球并形成了隐窝。换句话说,“迷你勇气”。
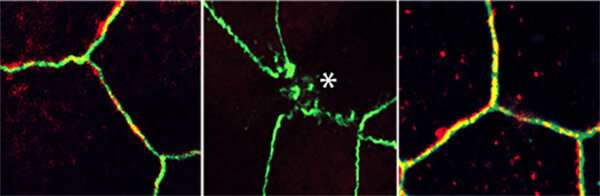
为了模拟泄漏的肠道条件,研究人员滚动了迷你齿轮以暴露肠道衬里的表面。然后它们洒在几种类型的细菌上,这强调了肠道衬里的连接,导致它们分开。
通过这个新模型,Ghosh, Das和团队证实了细胞间的连接是由先前确定的应激极性信号通路控制的。他们发现,随着年龄的增长和结直肠肿瘤的发展,保持肠壁完整的途径开始瓦解。他们还测量到,随着肠道屏障开始失效,炎症标志物的增加。
但研究小组发现,这种压力极性信号通路可以恢复。糖尿病药物二甲双胍激活AMPK,这是一种在应激极性信号通路中起关键作用的酶。研究人员证明,二甲双胍增强了迷你肠道的连接处,在受到细菌、衰老或肿瘤形成的压力时,会使肠道内壁收缩。一种测量应力-极性信号通路强度的方法是一种叫做咬合蛋白的分子的水平。在Ghosh和Das的实验中,与未处理的细胞相比,二甲双胍使occludin水平增加了6倍。
由于每个人源自不同的人,因此迷你肠道在其潜在的遗传和表观遗传学方面变化。这是一个力量,戈什说,也是一个限制。
她说:“很多研究都是在近亲繁殖的老鼠身上进行的,所以它们的基因是相同的,都关在同一个笼子里,吃同样的食物,为了从研究中排除这些变量。”“但每天实验室里的老鼠比同样的人或我们在诊所里看到的病人要标准化得多。在这里,我们的模型更好地代表了人性。另一方面,这也意味着每一个类器官都是它自己独特的实验。我们必须对许多类器官进行测试,才能做出任何声明,我们在研究中就是这样做的。”
接下来,研究人员想要进一步研究由肠漏引起的疾病。他们还计划在衰老、炎症性肠病、癌症和其他情况下测试各种收紧连接的方法,看看它们是否能减少或防止这些疾病的发生和发展。
“我觉得你很难找到一种疾病,其中全身炎症不是驾驶员,”DAS说。“这就是为什么,即使我们仍然不知道这么多的事情,我们对这一模型的广泛潜力和这些调查结果都可以兴奋,用于开发针对AMPK和应力 - 极性信号传导途径的个性化泄漏肠道治疗方法。”
进一步探索













用户评论