人工智能可能有助于预测对非小细胞肺癌全身治疗的反应

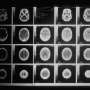
研究人员利用标准护理计算机断层扫描(CT)扫描晚期非小细胞肺癌(NSCLC)患者,利用人工智能(AI)训练算法来预测肿瘤对三种全身癌症治疗的敏感性。
这项研究发表在临床癌症研究哥伦比亚大学欧文医学中心放射学系的副研究科学家Laurent Dercle博士在美国癌症研究协会的一份杂志上发表了这篇文章
“放射科医生对接受全身治疗的癌症患者的CT扫描结果的解释本质上是主观的,”Dercle说。“这项研究的目的是训练尖端的人工智能技术来预测患者对治疗的反应,使放射科医生能够在疾病的早期阶段提供更准确和可重复的治疗效果预测。”
Dercle解释说,为了确定非小细胞肺癌患者是否对全身治疗有反应,放射科医生目前量化肿瘤大小的变化和新肿瘤病变的出现。然而,这种类型的评估可能是有限的,特别是在接受免疫治疗的患者中,他们可能表现出非典型的反应和进展模式,他指出。Dercle说:“较新的全身疗法促使对反应评估的替代指标的需求,这可以影响治疗决策。”
Dercle及其同事利用了多个II/ III期的数据临床试验评估非小细胞肺癌患者的全身治疗。这些患者接受三种药物中的一种治疗:免疫治疗药物纳武单抗(Opdivo)、化疗药物多西他赛(taxoere)或靶向治疗药物吉非替尼(Iressa)。研究人员回顾性分析了两项试验中92名接受纳武单抗治疗的患者的标准护理CT图像;在一项试验中,50例患者接受多西他赛;在一项试验中,46名患者接受吉非替尼治疗。
为了建立模型,研究人员使用了基线和首次治疗评估时的CT图像(吉非替尼治疗患者三周;接受纳武单抗或多西他赛治疗的患者为8周)。肿瘤根据每个试验的参考标准被分类为治疗敏感或治疗不敏感(纳武单抗和多西他赛队列的中位无进展生存期;吉非替尼治疗后手术标本分析。在所有三个队列中,患者被随机分为训练组或验证组。
研究人员利用机器学习开发了一个多变量模型来预测训练队列中的治疗敏感性。每个模型都可以根据基线时确定的最大可测量肺病变的变化预测从0(最高治疗敏感性)到1(最高治疗不敏感性)的评分。
由于吉非替尼队列的患者数量有限,研究人员建立并验证了一个使用抗egfr治疗的转移性结直肠癌患者队列(302人)的模型。然后利用在结直肠癌队列中确定的预测治疗敏感性的放射学特征,在非小细胞肺癌患者接受吉非替尼治疗的训练队列中建立模型。
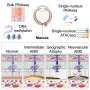
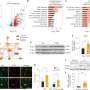
在所有队列中,共有8个放射学特征被用来建立三个预测模型。这些特征包括肿瘤体积、异质性、形状和边缘的变化。纳武单抗和吉非替尼模型都使用了四种放射学特征,而多西他赛模型使用了一种。
通过计算曲线下面积(AUC)来评估每个签名的性能模型其中,1分代表完美预测。在验证队列中,纳武单抗、多西他赛和吉非替尼预测模型的AUC分别为0.77、0.67和0.82。
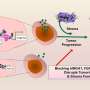
“我们观察到相似的放射组学特征预测了NSCLC患者的三种不同的药物反应,”Dercle说。“此外,我们发现确定转移性结直肠癌患者EGFR治疗敏感性的相同四个特征可以用于预测治疗敏感性病人转移性非小细胞肺癌。”
Dercle指出,放射学特征提供了增强临床决策的潜力。“随着人工智能,癌症成像可以从固有的主观工具转变为精确医学方法的定量和客观资产,”他说。
本研究的局限性包括样本量小。Dercle指出:“由于人工智能可以不断地从现实世界的数据中学习,因此在更大的患者数据集上使用人工智能将有助于我们识别新的模式,从而建立更准确的预测模型。”
更多信息:临床癌症研究(2020)。DOI: 10.1158 / 1078 - 0432. - ccr - 19 - 2942