Bin1缺陷损害脑细胞通信,内存整合

根据遗传变异的基因组研究,桥接集成器1是宾1,称为BIN1,是晚期疾病的第二个最常见的危险因素。然而,科学家们对这个蛋白质在大脑中表现不少。
现在,一个新的临床前研究发现,缺乏Bin1导致神经递质传播的缺陷,激活允许我们思考,记住和行为的脑细胞通信。由Gopal Thinakaran,博士,南佛罗里达大学卫生(USF Health)Morsani Matersani和Chicage of Chicago大学,这项研究于3月10日出版细胞报告。
阿尔茨海默病的约40%的人在纸张的高级作者博士博士博士博士博士博士博士中有大约40%的宾1基因 - 一股毛刺(核苷酸)中的三个变异。USF Health的分子药物Byrd Alzheimer的中心和义科医院神经科学研究的副院长在Morsani医学院。
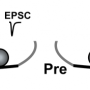
“我们的调查结果,Bin1在突触前沟通点定位,可以精确调节神经递质囊泡释放让我们更接近了解Bin1如何将其功能作为阿尔茨海默病的共同危险因素,“斯托纳坎博士说。”我们怀疑它有助于控制神经元沟通有效,可能对此产生深远的影响内存整合- 将最近学到的经历转化为长期记忆的过程。“
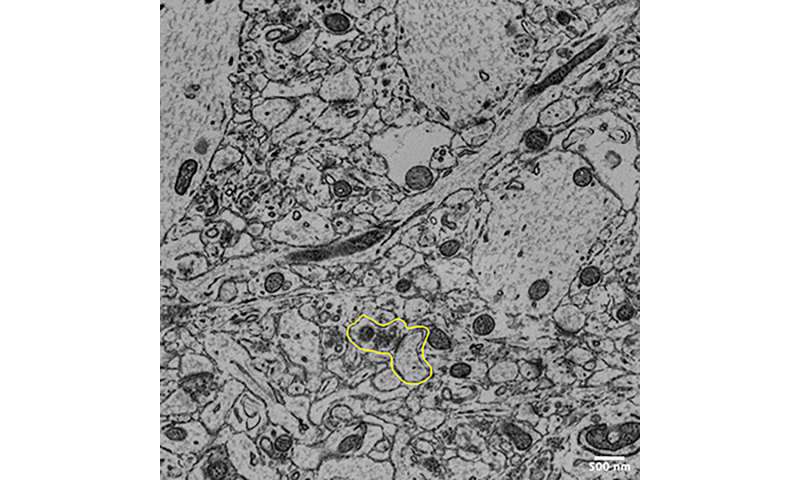
研究团队创造了一个鼠标模型其中Bin1基因选择性地灭活或敲除,以表征蛋白质在脑中的正常功能。特别是,它们使用先进的细胞和分子生物学技术来研究Bin1在与学习和记忆相关联的突触中的作用。
为了框架研究结果,有助于知道健康的人类大脑含有数十亿脑细胞(神经元),该脑细胞(神经元)在神经元之间的微小差距中处理和传递化学消息(神经递质)。在阿尔茨海默病的疾病大脑中,这种突触通信被摧毁,逐渐杀死神经元,最终导致记忆力陡峭下降以及痴呆症的其他迹象。Thinakaran博士说,最容易发生的Alzheimer在后期生活中最容易发生的阿尔茨海默氏症的个人是那些失去最多突触的人。
之间细胞报告研究亮点:
- 神经元中Bin1表达的丧失导致空间学习和记忆受损。也就是说,赤字改变了获取,存储,组织和使用的关于周围环境空间的有效信息。Bin1敲除小鼠比在莫里斯水迷宫中找到隐藏的平台在控制方面具有显着的难度。
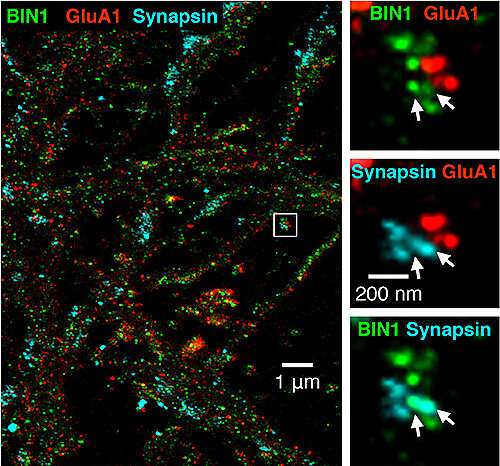
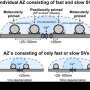
- 进一步分析区分该BIN1主要位于神经元的神经元定位,该神经元在突触(突触前位点)上发送神经递质,而不是居住在接受神经递质消息(突触位点)的那些神经元上。海马中的突触传递,一种主要与记忆相关联的脑区域,表明,来自囊泡的神经递质释放的劣化。囊泡是泡沫状载体,其将神经递质从突触前转移到后突触神经元。
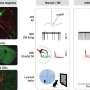
- 与对照相比,BIN1缺乏与突出小鼠突触小鼠中突触簇数的减少有关。
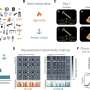
- 突触的3-D电子显微镜重建显示了Bin1敲除小鼠中对接和突触囊泡的停靠和储备池的显着积累。研究人员表明,这表明从他们的囊泡中释放神经递质的较慢(成功)释放。
该研究作者的结论是,他们的工作完全突出了突触前法规中神经元Bin1的非冗余作用,并“开启了未来调查Bin1作为阿尔茨海默病病理病理学的危险因素的新途径。”
进一步探索











用户评论