细胞相互注射的发现开启了对抗癌症的新途径
虽然大多数癌细胞被化疗杀死,但个体细胞敏感,因此一些癌细胞经常逃逸。因此,癌细胞之间的多样性是癌症治疗的问题。
以前的多样性被认为主要是由于遗传变异癌症细胞。然而,现在悉尼大学的研究人员发现了一种全新的癌细胞多样性来源,它具有深远的意义癌症治疗。
2012年,由悉尼大学牙科学院汉斯·佐尔纳教授领导的一个团队发表了一篇论文,称癌细胞会与周围环境交换内容正常细胞叫做成纤维细胞,但其机制直到现在还不清楚。
今天公布的结果生物物理期刊由Zoellner的团队终于解释了如何。
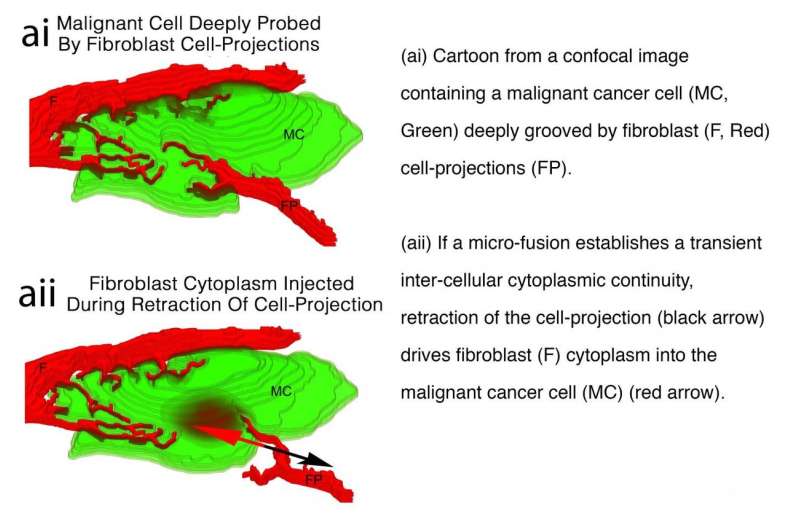
所有的细胞通过触角状的细胞投射不断地相互探测。作为细胞感知环境的一种方式,它们会向周围的细胞伸出触角,探测,然后缩回。当细胞投射收缩时,投射内的流体压力会短暂增加,以迫使细胞质(细胞内的胶状液体)返回细胞体。
学习细胞在延时电影中,佐尔纳教授注意到细胞的转移来自于细胞投影的收缩。
他推断缩回细胞突起和任何相邻细胞之间的瞬时微融合将允许从细胞突出物中注射到邻居中的细胞质,而不是返回成纤维细胞。
佐尔纳和他的团队在悉尼的医学和卫生学院工作,在纽约的纪念斯隆凯特琳癌症中心休假,他们通过结合数学模型、细胞实验和计算机模拟来验证这个想法。其结果是发现了一种以前似乎不为人知的生物学机制,现在称之为“细胞投射泵”。
在细胞投影泵送后,癌细胞变得更加激进
通过Zoellner的团队教授发布的单独工作,ZOELLNER团队的独立工作,也与纪念斯隆 - 肯特癌症中心合作,强调了细胞投影泵的重要性。他们发现了癌症细胞在细胞投影泵送之后,变得更加多样化,也更快地迁移。重要的是,初步结果显示出进一步的效果,抵抗化疗。
工作持续,Zoellner说:“这是一个全新的癌症目标。现在我们知道它正在发生,我们可以考虑试图阻止它,并努力更好的结果。
“这是一个艰难的项目,持续了19年,很难获得资金,但我很高兴有这么优秀的同事,并为我的团队的坚持感到自豪。”
进一步探索













用户评论