研究指出了杂散犬的证据,因为SARS-COV-2大流行的起源

自从SARS-COV-2爆发以来,科学家们一直在争先恐后地争夺原产地,以了解新的冠状病毒首先从动物宿主到人类跳跃,导致目前的大流行感染了全世界超过一百万人。
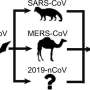
科学家一直在寻找蝙蝠之间的中间动物宿主,该蝙蝠众所周知,这些冠状虫病毒以及第一次将SARS-COV-2引入人类。
许多动物从蛇开始,最近开始,穿孔,都是作为可能的中间体出来的,但是从SARS-COV-2中孤立的病毒太分散了,暗示了一个普通的祖先 - 生活在20世纪60年代。
现在,渥太华大学生物学教授徐华夏教授,追踪不同物种的冠状病毒签名,提出了流浪犬 - 特别是狗肠 - 可能是目前SARS-COV-2大流行的起源。
“我们的观察结果允许形成SARS-COV-2的起源和初始传播的新假设,”夏天说。“SARS-COV-2的祖先及其最近的亲戚,蝙蝠冠状病毒感染了CANID的肠道,最有可能导致快速演变病毒在CANID及其跳进人类。这表明在对抗SARS-COV-2的斗士中监测SARS样冠状虫病毒的重要性。“
该研究结果显示在“期刊的高级访问”在线版中分子生物学和演化。
XIA已经长期研究了不同宿主的病毒的分子签名。当病毒侵入主持人时,他们的基因组经常通过其基因组内发现的变化和适应来抵抗并逃避主持人的免疫系统。
人和哺乳动物具有叫做ZAP的关键抗病毒哨蛋白,其可以通过防止宿主中的倍增并降解其基因组来阻止其轨道中的病毒。病毒靶标是在其RNA基因组内称为CpG二核苷酸的一对化学字母。CpG二核苷酸充当一个人的免疫系统用于寻求和破坏病毒的路标。ZAP巡逻人肺,并在骨髓和淋巴结中大量制作,免疫系统首先引用其攻击。
但已经表明病毒可以回来。单链冠状病毒,如SARS-COV,可以通过减少这些CPG路标来避免ZAP,从而使ZAP无能为力。对艾滋病毒,另一个RNA病毒的类似检查表明,它还利用了这种进化的技巧,以应对人类抗病毒防御。其中一种含义是病毒基因组的剩余CpG二核苷酸可能对病毒具有功能均值重要,并且可以作为改性的靶标,以减弱疫苗发育中的毒力。
“将病毒病原菌中的降低量减少为对公共卫生的威胁增加,而CPG的增加程度降低了这种病原体的威胁,”夏天说。“具有增加量的CPG量的病毒将更好地由主机定位免疫系统,并导致毒力减少,这将类似于天然疫苗。“
为了进行研究,XIA检查了所有1252个全长βAvirus基因组,迄今为止沉积在GenBank中。夏发现SARS-COV-2及其最密切相关的相对,蝙蝠冠状病毒(Batcov RATG13),其紧密的冠状病毒亲属之间的最低CPG。
“最引人注目的模式是在导致Batcov Ratg13的血管基因组CpG中的孤立但戏剧性的向下转移,其据报道,据报道,2013年云南省的蝙蝠(鼻孔Affinis)被取样,但仅被武汉病毒学研究所的测序2019年底,SARS-COV-2感染的爆发,“夏说。“该蝙蝠CoV基因组是SARS-COV-2的最接近的系统发育相对,共用96%序列相似性。”
“在这种情况下,不幸的是,Batcov Ratg13未在2013年进行测序,否则CPG的下卓可能由于两个强度含义而导致警告,”XIA说。“首先,病毒可能在具有高ZAP表达的组织中演变,其利用低CPG的病毒基因组。第二种,更重要的是,病毒的存活表明它已成功逃避ZAP介导的抗病毒防御。换句话说,病毒已经偷偷了,对人类危险。“
夏申请了他的CPG工具重新审视MERS的骆驼起源,发现那些感染骆驼的病毒消化系统还具有比感染骆驼呼吸系统的基因组CpG更低。
当他在患有狗的数据中检查了数据时,只有来自犬冠状病毒(Ccovs)的只有基因组,它在狗的全世界引起了高度传染性的肠疾病,具有类似于在SARS-COV-2和Batcov Ratg13中观察到的基因组CpG值。其次,像骆驼一样的CANID也有冠状病毒感染他们的消化系统,CPG低于感染呼吸系统(犬呼吸道冠状病毒或属于Betacov的CRCOV)。
另外,已知的SARS-COV-2进入细胞的细胞受体是ACE2(血管紧张素I转化酶2)。ACE2在人体消化系统中,在小肠和十二指肠中的最高水平,肺部表达相对较低。这表明哺乳动物消化系统可能是由冠状病毒感染的关键靶标。
“这与解释的符合性,即SARS-COV-2中的低CPG被SARS-COV-2在哺乳动物消化系统中的祖先获得的,并且通过最近的报告进一步证实了Covid-19的高比例,进一步证实了患者也患有消化不足感,“夏说。“事实上,48.5%呈现出消化症状作为他们的主要投诉。”
人类是XIA的唯一观察到的其他宿主物种,产生具有低基因组CPG值的冠状病毒基因组。In a comprehensive study of the first 12 COVID-19 patients in the U.S., one patient reported diarrhea as the initial symptom before developing fever and cough, and stool samples from 7 out of 10 patients tested positive for SARS-CoV-2, including 3 patients with diarrhea.
通常会观察到CANID,以舔他们的肛门和生殖器区,不仅在交配过程中,而且在其他情况下。这种行为将促进从消化系统到呼吸系统的病毒传播和胃肠病原体和呼吸道和肺病原体之间的交换。
“在这种情况下,蝙蝠冠状病毒(BATCOV RATG13)与其在Genbank(MN996532)中的基因组序列中被分离出来的显着性,从粪便拭子中分离出来。这些观察结果与SARS-COV-2的假设一致在与肠道相关的哺乳动物肠或组织中演变。“
XIA的另一个研究涉及最近从植物林中分离的病毒。最近已被隔离和测序九个SARS-COV-2类似基因组,并从Pangolin中排序并存放在GisaID数据库(Gisaid.org)中。“具有最高序列覆盖的(GISAID ID:EPI_ISL_410721)的ICPG值为0.3929,接近可用SARS-COV-2基因组中观察到的CPG值的极低末端。因此,SARS-COV-2,BatcovRATG13和来自Pangolin的父母可以具有低CPG的共同祖先,或者具有趋同的低CPG值。“
根据他的结果,夏呈现出一种情景,其中冠状病毒首先从蝙蝠传播到吃蝙蝠肉的流浪狗。接下来,对病毒RNA中的CPG可能是强烈的选择基因组在Canid肠中导致病毒的快速演变导致降低基因组CpG。最后,降低的病毒基因组CpG允许病毒逃避人ZAP介导的免疫应答,并成为严重的人道病原体。
“虽然SARS-COV-2的特定起源对当前的世界卫生危机具有重要兴趣,但这项研究更广泛地表明,可以通过考虑宿主基因组的相互作用,包括选择性的宿主防御的相互作用来揭示病毒进化的重要证据宿主组织施加的压力病毒基因组作文,“夏说。











用户评论