您的基因可以确定冠状病毒是否将您送入医院
 Prot reimage via Wikimedia Commons, CC BY-SA" width="800" height="530">
Prot reimage via Wikimedia Commons, CC BY-SA" width="800" height="530">
当有些人感染冠状病毒时,他们只会出现19009年的轻度或无法检测的病例。其他人则遭受严重的症状,如果他们根本可以生存几周,为呼吸器呼吸数周。
尽管全球科学努力,医生还是仍然缺乏清晰的图片为什么这是。
可以遗传差异解释我们在Covid-19的症状和严重程度中看到的差异?
为了测试这一点,我们使用计算机模型分析已知遗传变异在人免疫系统。我们的建模结果表明,实际上,人们的DNA存在差异,可能会影响他们对SARS-COV-2感染的反应能力。
我们做了什么
当病毒感染人类细胞,人体通过打开什么基本是反病毒警报系统来做出反应。这些警报识别病毒入侵者,并告诉免疫系统发送细胞毒性T细胞(一种白细胞类型),以破坏感染细胞并希望减缓感染。
但是并非所有警报系统都是平等的。人们有不同版本的相同基因(称为等位基因),其中一些等位基因更多比其他病毒或病原体敏感。
为了测试此警报系统的不同等位基因是否可以解释对SARS-COV-2的免疫反应的某些范围,我们首先从一个蛋白质中检索了所有蛋白质的列表在线数据库。
然后,我们获取该列表,并使用现有的计算机算法来预测不同版本的抗病毒警报系统检测到这些冠状病毒蛋白的良好。
为什么重要
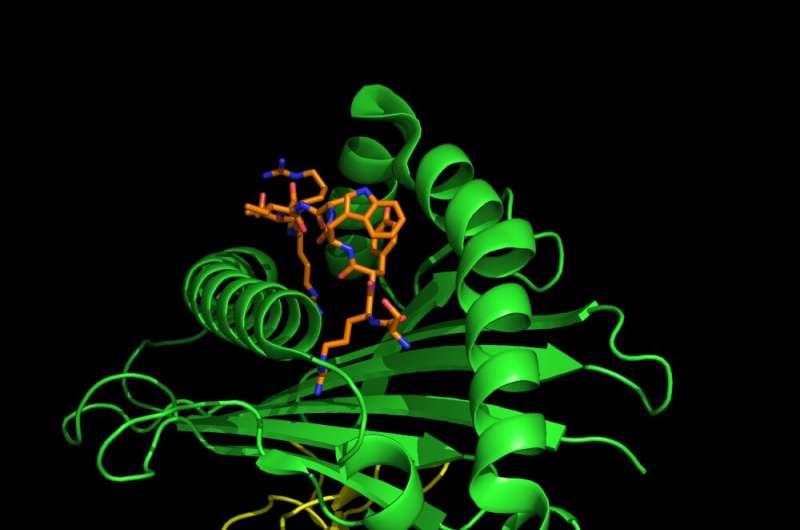
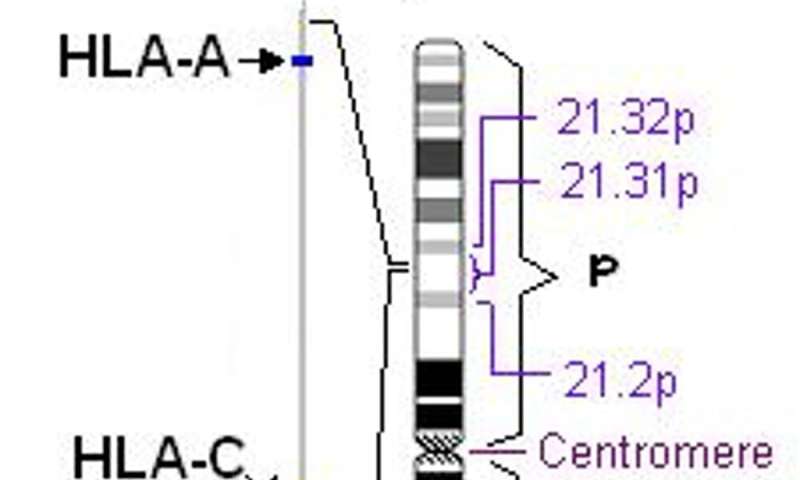
我们测试的警报系统的一部分称为人类白细胞抗原系统或HLA。每个人都有构成其HLA类型的基因的多个等位基因。每个等位基因编码不同的HLA蛋白。这些蛋白质是警报系统的传感器,并通过与各种构成冠状病毒部分的氨基酸的链结合(氨基酸的链)来找到入侵者。
一旦HLA蛋白与病毒或病毒结合,它就会将入侵者运输到细胞表面。该“标记”细胞被感染,并从那里从那里杀死细胞。
通常,一个人的HLA可以检测到的病毒的肽更多的肽,免疫反应更强。将其视为更敏感的传感器警报系统。
我们的建模结果预测,某些HLA类型与大量SARS-COV-2肽结合,而其他HLA类型则与少数结合。也就是说,某些传感器可能比其他传感器更适合SARS-COV-2。如果是的,那么一个人的特定HLA等位基因可能是其免疫反应对COVID-19的有效性的一个因素。
由于我们的研究仅使用计算机模型来做出这些预测,因此我们决定使用2002-2004 SARS暴发的临床信息来测试结果。
我们发现等位基因在识别SARS和SARS-COV-2方面的有效性相似。如果HLA等位基因在识别SARS-COV-2方面似乎很不好,那么认识SARS也很糟糕。我们的分析预测,在SARS-COV-2和SARS-COV方面,一个称为B46:01的等位基因尤为不好。果然,以前的研究表明,这等位基因倾向于有更多严重的SARS感染与具有其他版本的HLA基因的人相比,病毒载荷更高。
下一步是什么?
基于我们的研究,我们认为HLA基因的变异是许多COVID-19患者感染严重程度巨大差异的解释的一部分。HLA基因中的这些差异可能不是影响COVID-19的严重程度的唯一遗传因素,但它们可能是拼图的重要部分。重要的是要进一步研究HLA类型如何在临床上如何影响COVID-19的严重程度,并使用实际病例测试这些预测。了解HLA类型的变异如何影响COVID-19的临床过程可能有助于识别出较高风险的人。
据我们所知,这是第一个评估广泛HLA等位基因的病毒蛋白之间关系的研究。目前,我们对许多其他病毒与HLA类型之间的关系知之甚少。从理论上讲,我们可以重复此分析,以更好地了解当前或可能感染人类的许多病毒的遗传风险。