新的肝癌研究以非癌细胞为靶点来抑制肿瘤生长
根据Celeste Simon博士领导的研究小组的新研究,“Senotherapy”是一种用小分子药物治疗“衰老”细胞,或那些不再进行细胞分裂的细胞,在动物模型中钝化肝脏肿瘤的进展。他是宾夕法尼亚大学佩雷尔曼医学院的细胞和发育生物学教授,也是艾布拉姆森家族癌症研究所的科学主任。这项研究发表在自然细胞生物学。
西蒙说:“这种疗法以前从未在肝癌上尝试过。”“在我们的模型中,所谓的‘senolytic’therapy极大地减轻了疾病负担,即使是晚期疾病。”
人肝细胞中FBP1酶的缺失显著增加了肿瘤的生长。此前的研究表明,FBP1水平在1期肿瘤中降低,并随着疾病进展进一步降低。在这项研究中,Simon和她的团队使用rna测序数据确定FBP1在最常见的肝癌(肝细胞癌)中普遍低表达,而不考虑潜在的原因,如肥胖、酗酒和肝炎。
肝细胞中FBP1的缺失激活了邻近的肝“星状细胞”,星状细胞占肝质量的10%,导致纤维化(组织瘢痕)和随后的星状细胞衰老,两者都会促进肿瘤的生长。研究人员发现,这些衰老的星状细胞可以被senolytics选择性靶向,包括Navitoclax(已经在其他疾病的临床试验中,如恶性血液系统疾病),以钝化由肝细胞特异性FBP1缺失驱动的肿瘤进展。
该研究小组首次提供了FBP1在肝脏中作为一种真正的代谢肿瘤抑制因子的遗传证据,并证明了它的丢失肝细胞由于对肿瘤微环境中的其他细胞的影响而促进肿瘤的生长。
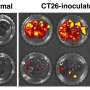
使用基因工程小鼠模型,研究小组排除了fbp1,发现在致癌基因介导的、饮食和其他形式的肝细胞癌中,疾病进展更快,肿瘤负担大大增加。
“肝癌的情况是非常可怕的,一旦你超过了一定的阶段,可用的治疗是有限的,如果有的话,”西蒙说。“随着肥胖率继续上升,病毒感染继续成为一个问题,肥胖率将会越来越高肝癌目前几乎没有治疗选择。而由于FBP1在肾癌中也失去了活性,FBP1缺失可能普遍适用于一些人类癌症。我们senotherapy的独特之处在于,我们专门针对肝癌环境中的其他细胞,而不是癌细胞本身。”
据研究人员称,下一步将开始在临床环境中测试这些治疗方法。
进一步探索













用户评论