科学家研究血细胞分化的表观遗传机制
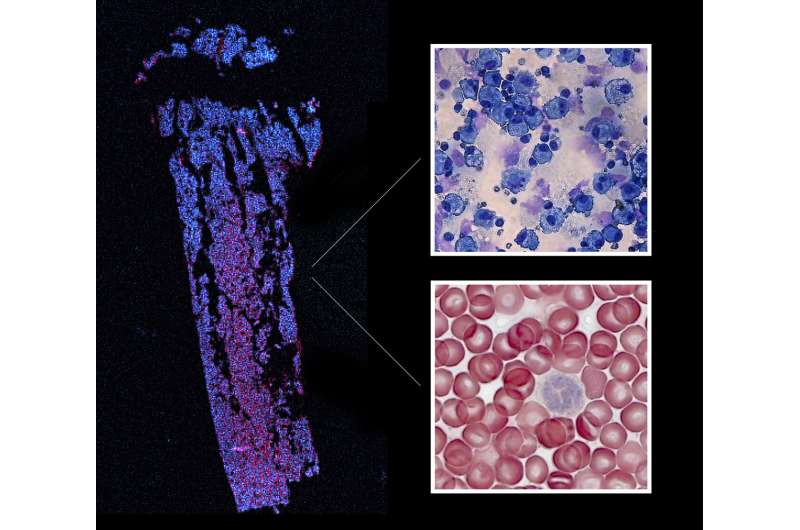
平均而言,人体含有35万亿红细胞(RBC)。大约三百万这些小盘形电池在一秒钟内死亡。但在第二个中,还产生相同的数字来维持活性RBC的水平。有趣的是,所有这些细胞都经历了一种称为红细胞的多级分化过程。它们从造血干细胞(HSC)开始,每个血细胞的前体,包括所有类型的免疫细胞,然后将其分化为多能祖细胞(MPPS),然后是专业化进入成熟红细胞的过程。
如果这种分化过程失败了,就会对我们的健康有害。例如,如果很少的造血干细胞选择遵循红细胞路线图,个体将容易发展为贫血。另一方面,免疫细胞路线图的异常与白血病的发生有关。
早期造血的表观遗传调节
在弗赖堡的免疫生物学和表观遗传学MPI的Asifa Akhtar实验室调查了什么管理血液的分化过程细胞。现在,研究小组已经确定了MOF酶,一种表观遗传调节器,是如何协调造血干细胞在红细胞生成中的命运的。
Asifa Akhtar说:“控制细胞发育过程的最重要的内在线索之一是染色质景观的调节。”在我们的细胞中,DNA被组蛋白包裹,形成染色质结构。这种包装在细胞类型特异性基因调控中起着至关重要的作用,当然,在红细胞分化中也是如此。在默认状态下,染色质不是“允许的”,这意味着基因处于关闭状态。但是改变组蛋白可以打开染色质,促进基因表达。
表观调控因子引导造血干细胞走上正确的道路
已知酶MOF通过在一个特定部位(K16ac)上乙酰化H4组蛋白直接触发染色质的“开口”。当实验室在小鼠的促红细胞生成期间跟踪MOF占用时,他们发现酶通过调节HSC和RBC祖细胞的染色质可用性来动态地调节红细胞产物。“我们的数据表明,血细胞发育过程中MOF的正确剂量和时序对于激活红霉发育计划的激活是必不可少的。该过程确保了红细胞分支的正确转录因子网络,”首先说-author cecilia pessoa rodrigues。
马克斯·普朗克的研究人员确信,这些发现可能意味着我们对红细胞系承诺的理解有相当大的进展,并可能为白血病或贫血等疾病提供新的治疗方法。尽管人类MOF缺失的确切后果仍未得到答复,但已知的是,表观遗传调节因子的平衡和控制活动对造血细胞的正常发育是必不可少的。“MOF水平低与急性髓系白血病(AML)有关并不奇怪。我们预计这可以用染色质乙酰化失衡来解释,这对正常造血所需的相关因素至关重要。揭示正确的水平染色质可访问性,随后,微调分化轨迹的基因监管机制将深入了解健康和患病状态的血缺陷,“Asifa Akhtar说。
进一步探索











用户评论