人类急性髓性白血病的发现可以为新治疗提供新的途径
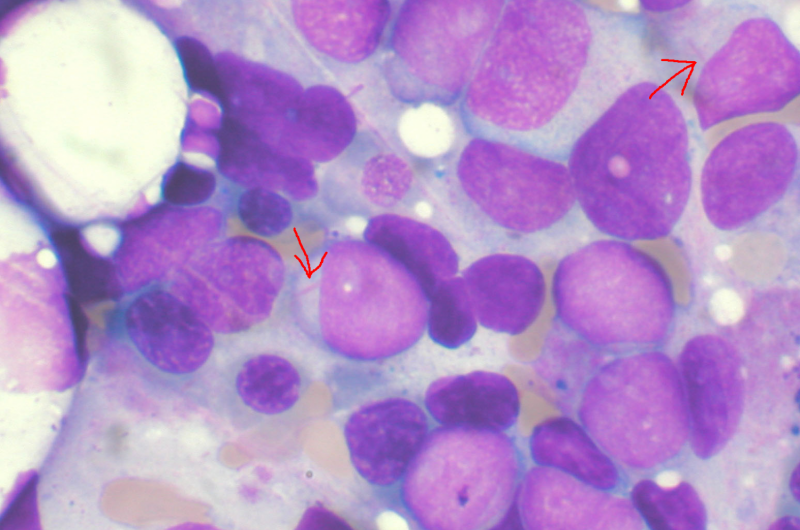
西奈山的研究人员发现,人类急性髓性白血病(AML)干细胞依赖于称为Runx1的转录因子,可能提供新的治疗目标,以实现医疗进展受限的持续剩余疏忽甚至治愈。
在六月发表的一项研究中细胞的报道,该团队描述了它们如何将诱导的多能干细胞与AML的患者一起用于在实验室中重建白血病干细胞生物学,揭示AML白血病干细胞一旦转录因子被击倒或删除就会失去白血病性质。研究人员进一步表明来自其他患者的AML细胞依赖于Runx1。
“我们开发了一种新的AML白血病干细胞模型,使我们能够比以往更详细地研究这些细胞,导致意外发现白血病干细胞对转录因子RUNX1的特定依赖性,”医学博士、博士生、肿瘤科学副教授Eirini Papapetrou说。他是西奈山伊坎医学院的研究员,也是这项研究的资深作者。“进一步挖掘,我们发现早期研究表明RUNX1表达是急性髓系白血病患者预后不良的一个标记。我们的工作现在可能提供了一种解释,即RUNX1需要维持白血病干细胞,从而使白血病增殖。”
急性髓性白血病是一种血液和骨髓的癌症,骨髓是骨骼内的海绵状组织,血液细胞在其中生成。急性髓系白血病,主要影响白人血细胞是成人最常见的白血病之一,在美国每年有超过20,000个新诊断的病例。尽管近年来已经推出了几种针对这种疾病的新药,但它们未能显著改变患者的预后或生存期。
Papapetrou博士是第一批衍生患者特异性诱导多能干细胞的研究者之一,并在疾病建模中使用它们,以更好地理解机制急性髓系白血病并确定有希望的新的治疗靶点。诱导多能干细胞(Induced pluripotent stem cells)是由成体细胞产生的,几乎可以分化成体内任何类型的细胞,这使得它们不同于胚胎干细胞,而且在某些方面更适合于胚胎干细胞。通过使用诱导多能干细胞帕佩特鲁博士和她的研究团队能够重现白血病干细胞的状态,这是很难用传统模型捕捉和研究的。她解释说:“我们的模型使分离和培养白血病干细胞在很长一段时间内变得更加容易,这意味着我们可以获得大量的白血病干细胞用于继续进行研究。”
该工作揭示了其他有趣的基因,似乎在白血病干细胞中的Runx1效应的调解中发挥作用。最突出的是TSPAN 18,这是哪种科学家认为可以证明是一种比RunX1更具吸引力的治疗靶,因为作为细胞表面蛋白,它可以靶向抗体或嵌合抗原受体(轿厢)T细胞方法。Tspan 18和其他躺在Runx1下游的候选基因可能是Papapetrou博士实验室调查的未来科目,该学科致力于研究血液疾病,特别是骨髓性恶性肿瘤。
事实上,实验室在人类白血病干细胞方面的进展对围绕白血病干细胞治疗靶向的整个领域有更广泛的影响。“我们正在证明,如果不解决白血病干细胞问题,就不能明显地影响白血病细胞“Papapetrou博士强调,补充说她的工作已经提供了数据集和表征的AML基因签名白血病干细胞这对未来的研究至关重要。“在这个早期阶段或者我们的工作会导致大量改进或可能是AML的治疗时,这是不可能的,”她说,“但我们看到的结果是非常有前途和强调这一巨大潜力场地。”
进一步探索









用户评论