抗COVID-19单克隆抗体进入临床试验
2020年6月5日,中国的国家医疗产品管理局(NMPA)正式批准了中国科学院微生物研究所的研究团队开发的全人单克隆抗体(MAB)的临床试验(IMCAS)。
第一阶段临床试验将在健康的人类中进行安全和适当剂量进行。这也是在非人灵长类动物模型评估后健康人治疗人员在健康人中的第一个临床试验。
自1月中旬以来,IMCAS组织了许多研究和技术团队来对抗Covid-19,包括延京华教授和高福(乔治福高)。
从COVID-19恢复期患者中分离和鉴定了数十个完整的人mAb基因。经过反复测试和比较,筛选出两种理想的特异性单克隆抗体,并于2月底高效中和了SARS-CoV-2。
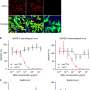
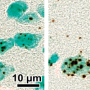
研究人员用恒河猴模型评估了单克隆抗体的效力。结果表明,该中和单抗有效阻断了SARS-CoV-2的感染,显著降低了新病毒的负荷量新冠病毒在恒河猴的呼吸道中,并受到病毒感染引起的肺部损伤的影响。
Covid-19在世界各地迅速传播,受感染的人数超过660万。世界各地的科学家正在努力寻找对病毒有效的药物,但仍然没有批准的药物。
中和抗体是靶靶病原体并阻止它们侵入细胞的特异性免疫球蛋白类型。报告的MAB代表了一种为SARS-COV-2开发的创新特定药物。这些MAB的这些临床试验带来了新的希望来抑制病毒的传播。
治疗性单克隆抗体的开发是基于病毒-宿主相互作用基础研究的突破。与中国科学院武汉病毒学研究所、人民解放军总医院、首都医科大学疾病预防控制中心、北京地滩医院等单位的研究人员合作,发表了一篇论文研究论文抗SARS-CoV-2全人源单克隆中和抗体自然,在2020年5月26日。













用户评论