这些发现削弱了神经连接中大小等于强度的观念
当神经元(称为突触)之间的连接不能对经验作出适当的反应时,学习、记忆和行为障碍就会出现。科学家们已经研究这种“突触可塑性”几十年了,但麻省理工学院皮考尔学习与记忆研究所的研究人员的一项新研究强调了它发生的一些基本机制的一些令人惊讶的地方。研究进一步表明,弄清这些令人惊讶的现象背后的原因,可能会产生治疗导致自闭症的脆性X染色体障碍的新方法。
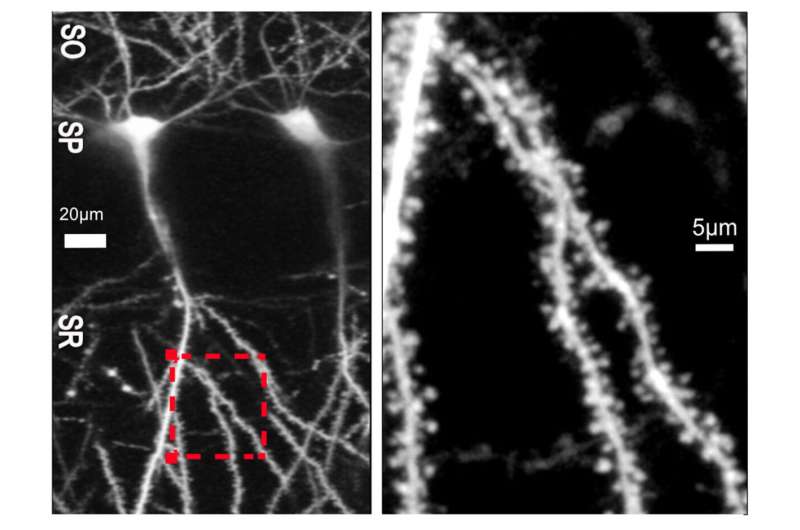
两种经典的形式突触可塑性突触是变强还是变弱支撑它们的微小脊椎结构是变大还是变小。长期以来,该领域的工作假设是,这些功能和结构的变化是密切相关的:增强伴随着脊柱尺寸的增加,减弱先于脊柱收缩。但这项研究发表在《分子精神病学》补充了具体的证据来支持最近的一个观点,该观点得到了其他近期研究的支持,即这些相关性并不总是正确的。
脑与认知科学系皮考尔教授、该研究的资深作者马克·贝尔(Mark Bear)说:“我们看到了结构与功能之间相关性的瓦解。”“一个结论是,你不能用脊柱的大小作为突触强度的代表——你可以用大球状的脊柱来代替弱突触。”我们并不是唯一这样做的人,但这项研究的新结果非常清楚。”
该研究的共同主要作者是前实验室成员Aurore Thomazeau和Miquel Bosch。
维度的分解
为了进行这项研究,该团队在两种不同的条件下(典型的神经啮齿动物和基因突变导致脆性X染色体的啮齿动物)通过两种不同的神经受体(称为mGluR5和NMDAR)刺激了小鼠的可塑性蛋白质FMRP会导致其他蛋白质的过度合成,导致大脑中海马区(记忆形成的关键区域)的突触过度减弱。
这项研究的第一个惊喜是,激活mGluR5受体会导致这种弱化,称为长期抑郁(LTD),但并没有导致任何脊柱脆性X染色体小鼠或对照组小鼠收缩至少一小时。换句话说,被认为是伴随着功能变化的结构变化实际上并没有发生。
在NMDAR的案例中,两种形式的可塑性确实同时发生,无论是在对照组还是脆弱的X啮齿动物中,但在表面之下隐藏着更多的意外,进一步分离了功能和结构的可塑性。当研究小组阻断NMDAR突触中的离子流(因此也就阻断了电流)时,这只是阻止了突触的减弱,而不是收缩。为了防止对照组老鼠的萎缩,研究人员必须做一些不同的事情:直接抑制蛋白质合成或通过抑制一种名为mTORC1的调节蛋白。
贝尔说:“这让我们很吃惊。”“我们正在积极跟进,以便更好地理解这种信号。”
脆性X的新机会
贝尔说,如果这项研究中的一些惊喜是破坏性的,那么另一个惊喜可能会为治疗脆性X染色体提供新的希望。这是因为贝尔的实验室一直专注于干预mGluR通路来治疗脆性X染色体,而涉及NMDAR的新实验可能揭示了另一种途径。
当研究小组试图通过抑制蛋白质合成或mTORC1来阻止脆性X啮齿动物的脊柱萎缩时(就像他们在对照组中做的那样),他们发现它没有起作用。就好像已经有太多的蛋白质促进了收缩。该团队甚至能够在对照组中复制这种脆性X现象,首先刺激mglur5 -然后过量蛋白质合成然后跟进NMDAR的激活。
作为对这一谜团和疾病的承认,贝尔已经开始将这种推测的潜在促缩分子称为“蛋白质x”。
“问题是什么是蛋白质X,”贝尔说。“有强有力的证据表明,有一种快速翻转的X蛋白正在对脆弱的X蛋白造成严重破坏。我们很高兴能找到它。”
进一步探索













用户评论