化合物通过靶向关键病毒酶来阻止SARS-CoV-2的复制
由于来自Covid-19大流行山的死亡人数,全世界科学家们继续推动他们的有效治疗和疫苗,为高度传染性的呼吸道病毒。
南佛罗里达大学卫生(USF Health)Morsani医学科学家最近与亚利桑那大学药房同事合作,鉴定了几种现有化合物,阻止了Covid-19病毒(SARS-COV-2)的复制人类细胞在实验室里生长。这些抑制剂都表现出与a病毒蛋白对病毒的扩散能力至关重要。
研究小组的药物发现研究于6月15日发表细胞研究这是一本影响力很大的《自然》杂志。
最有前途的毒品候选者 - 包括FDA批准的丙型肝炎药物Boceprevir和一种称为GC-376 - 靶向SARS-COV-2主要蛋白酶(M的调查兽医抗病毒药物(M)箴),它是一种酶,可以把病毒入侵人体细胞时产生的长链蛋白质切下来。没有米箴,病毒不能复制和感染新的细胞。这种酶已经被验证为最初SARS和MERS的抗病毒药物靶点,这两种病毒在基因上与SARS- cov -2相似。
“对于像COVID-19这样快速出现的传染病,我们没有时间从头开始开发新的抗病毒药物,”《细胞研究》论文的合著者、旧金山大学健康学院分子医学副教授陈宇博士说。“很多优秀的候选药物已经在那里作为一个起点。但是,有了像我们这样的研究提供的新信息和当前的技术,我们可以更快地帮助设计更好的(重新利用)药物。”
在流感大流行之前,陈博士利用他在基于结构的药物设计方面的专业知识,帮助开发了针对细菌酶的抑制剂(药物化合物),这些酶会导致对某些常见抗生素(如青霉素)产生耐药性。现在,他的实验室专注于x射线晶体学和分子对接等先进技术,以寻找阻止SARS-CoV-2的方法。
米箴陈竺说,由于这种酶在冠状病毒的生命周期中发挥着重要作用,而人类体内缺乏类似的蛋白酶,因此它是研发抗COVID-19药物的一个有吸引力的目标。他解释说,由于人体内没有这种酶,针对这种蛋白质的药物产生副作用的可能性较小。

下面描述了亚利桑那州 - USF大学卫生组织核心卫生团队的四名领先的毒品候选人,作为战斗Covid-19的最佳(最有效和具体)。在筛选超过50个现有的蛋白酶化合物后,这些抑制剂升至顶部,用于潜在重新施加:
- Boceprevir是一种治疗丙型肝炎的药物,是FDA批准的四种化合物中唯一的一种。陈竺表示,目前已知boceprevir的有效剂量、安全性、配方以及机体对药物的处理方式(药代动力学),这将大大加快boceprevir进入COVID-19临床试验所需的步骤。
- GC-376是一种用于治疗猫体内一种致命冠状病毒毒株的实验性兽医药物,这种毒株会导致猫传染性腹膜炎。该药剂是M箴但在开始人体试验之前,还需要在SARS-CoV-2动物模型上进行试验。陈博士和他的博士生Michael Sacco测定了由M束缚的GC-376的x射线晶体结构箴并且使用3D计算机建模的化合物和病毒酶之间的分子相互作用。
- Calpain抑制剂II和XII,半胱氨酸抑制剂在过去进行了癌症,神经变性疾病和其他条件,也表现出强烈的抗病毒活性。他们能够双重抑制m箴研究人员报告说,钙蛋白酶/组织蛋白酶表明,这些化合物可能包括抑制耐药性的额外好处。
四种化合物均优于其他M箴陈博士说,以前被确定为适合临床评估治疗SARS-CoV-2的抑制剂。
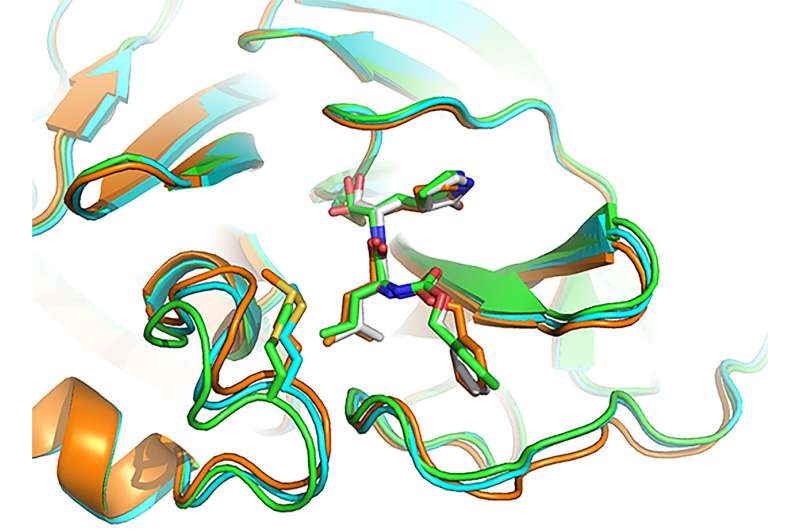
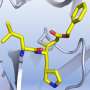
有一种很有前途的候选药物可以在不破坏健康细胞的情况下杀死或削弱病毒,它可以紧贴在病毒蛋白受体独特形状的“结合口袋”里。GC-376在符合(补充)目标M的形状方面工作得特别好箴陈博士说。他用锁(捆绑口袋或受体)和钥匙(药物)作类比,“GC-376是目前为止最合适的钥匙,”他补充说。“我们的模型显示,当抑制剂与SARS-CoV-2主蛋白酶表面的活性位点结合时,它是如何模拟原始的肽底物的。”
这种抑制剂并没有像底物通常那样促进病毒酶的活性,而是显著降低了帮助SARS-CoV-2复制自身的酶的活性。
可视化的3-D抗病毒化合物和病毒蛋白之间的相互作用提供了一个更清楚的了解如何M箴陈竺说,这是一项复杂的工作,从长远来看,可能导致设计新的COVID-19药物。与此同时,他补充说,研究人员专注于通过调整现有的冠状病毒候选药物,以提高其稳定性和性能,更快地将有针对性的抗病毒治疗送到第一线。
陈博士与首席研究员王军博士(博士,UA药理学和毒理学助理教授)一起进行了这项研究。这项研究部分得到了美国国立卫生研究院(National Institutes of Health)的资助。














用户评论