磷蛋白生物标志物引导癌症治疗
癌症治疗中的精准医疗利用癌细胞的基因变化来为个别患者选择最好的治疗方法。
现在研究人员由詹姆斯Bibb,博士,伯明翰大学手术教授,建议使用翻译后修改分析的更广泛的镜头来识别可能允许更精确预测的癌症驱动程序的新生物标志物患者对治疗的反应。在发表的一项研究中国家科学院的诉讼程序,他们证明了这种诊断替代因异常被激活的神经内分泌肿瘤的诊断替代品蛋白激酶叫CDK5。
“我们的研究结果表明,精密医学是治疗稀有和顽皮症癌症的可实现目标,”博士,博士的原则作者和UAB的BIBB实验室的博士后研究员说。
“相同的方法,”BIBB说,“可以适应鉴定其他肿瘤司机的标记。作为癌症类型的癌症类型的数量升高,并且随着具有选择性靶向CDK5的药物朝向诊所移动,这种诊断治疗耦合系统的平移潜力将是广泛的。“
UAB研究人员现在与国家癌症研究所合作,使该团队发现的生物标志物调整到临床上适用的诊断测定中,并将靶向这些途径的新药物转移到临床试验。
Cdk5是一种磷酸化的周期蛋白依赖性激酶目标蛋白质作为细胞中信令序列的一部分。CDK5活性主要限于神经元细胞,在那里它对于中枢神经系统的开发和学习和记忆等认知过程至关重要。
在PNA纸,卡特,BIBB及其同事首先检查了多种神经内分泌肿瘤和癌症类型的样本,发现CDK5及其活化剂P35和P25表征了所有神经内分泌肿瘤的大部分。此外,CDK5抑制剂阻断肿瘤的生长,表明CDK5活性是这些癌细胞生长的主要因素。
为了寻找生物标志物,研究人员首先使用了髓质甲状腺癌的独特鼠标模型,或MTC,其肿瘤的生长可以打开或关闭。然后,它们在被捕和生长的MTC之间寻找磷酸化肽片段的全局差异。进一步使用将阻断磷酸化的短干扰肽进一步检查生长MTC中的50个最高度上调的磷酸化位点。发现十五种干扰肽抑制神经内分泌的生长癌细胞但不是正常的成纤维细胞,其鉴定了癌细胞生长所需的CDK5的下游靶标。显示CDK5信号传导级联的15个靶标显示来自与常见癌症机制相关的蛋白质。
产生磷酸化状态特异性抗体以检测这些位点中的六个和预先鉴定为CDK5靶标的其他位点。八个位点中的六个位点显示了人类神经内分泌癌细胞系中CDK5抑制剂的剂量依赖性减少,这意味着肽来自蛋白质的磷酸化磷酸化。“我们的整体数据表明,这六种蛋白质的磷酸化对于驱动这些癌症至关重要,并且依赖于CDK5活性。它还表明这些磷酸化位点可以用作许多类型的CDK5驱动的神经内分泌肿瘤的生物标志物,”BIBB说。
三种表现出人体MTC患者肿瘤队的显着高度和与CDK5表达的正相关;在肿瘤样本的一小部分中,另一个增加了与CDK5表达的正相关。测试的近四分之三的患者肿瘤显示出升高的CDK5水平;但只有五分之一的CDK5途径活性的所有四个生物标志物的升高,强调蛋白质的存在与该蛋白质的功能不相关。
研究人员随后发现,在不同的MTC动物模型中,Cdk5抑制抑制了肿瘤的生长。然后,他们测试了患者来源的异种移植模型是否存在假定的Cdk5生物标记物,结果显示,使用Cdk5抑制剂治疗后,两种生物标记物阳性的癌症的生长下降,而两种生物标记物阴性的癌症的肿瘤生长没有下降。这些结果有力地支持了生物标志物预测抗cdk5治疗反应的能力。
然而,肿瘤未见消退,较高水平的Cdk5抑制剂具有相当的毒性。因此,研究人员测试了一种名为白质小体(LKs)的仿生纳米颗粒给药系统。白质小体是由合成磷脂和白细胞膜提取物合成的。LKs具有靶向肿瘤炎症环境的能力,它们的白细胞膜蛋白可以伪装它们,使其不被免疫系统清除。
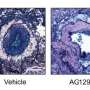
LKS在小鼠中显示出MTC肿瘤的局部化增加,在那里它们可以递送较低剂量的CDK5抑制剂,其具有与更高的毒性剂量的免费CDK5抑制剂具有相同的有效性。
“目前的研究表明,Cdk5可能是所有神经内分泌的至少一部分肿瘤“Bibb说”。“该研究还识别了一组基于磷酸化的生物标志物,这表明不仅存在CDK5途径组分,而且CDK5正在主动调制信号网络和调节癌症生理机能。
“为了在临床上有用,用于检测这些生物标志物的抗体需要开发成一种易于使用的、可靠的定量分析方法生物标志物患者肿瘤的水平,最好是在相对较小的样本,如核心活检。”
进一步探索












用户评论