在一项新的研究中,一种ALS基因的沉默安全地传递给了患者

马萨诸塞大学医学院和麻省总医院是第一个用合成microRNA安全地治疗两名研究参与者的机构,该合成microRNA被输送到脊髓液中,旨在抑制人类致病基因。治疗的细节,针对导致ALS的突变SOD1基因,出现在新英格兰医学杂志.
这项研究由医学博士小罗伯特·h·布朗(Robert H. Brown Jr.)、医学研究的Leo P.和Theresa M. LaChance主席、神经学教授和UMMS神经治疗学项目主任领导;ob欧宝直播nbaUMMS儿科副教授Christian Mueller博士与Sean M. Healey & AMG ALSob体育开户网址中心主任Merit Cudkowicz医学博士、MGH神经病学主任和哈佛医学院神经病学Julianne Dorn教授合作;詹姆斯·d·贝里,医学博士,公共卫生硕士,渐冻人症科学温斯洛普家族学者,MGH渐冻人症和运动神经元疾病部门负责人,MGH肖恩·m·希利和AMG渐冻人症中心。
“这项研究最大的收获是,我们提供了一种新的沉默基因治疗并有效地抑制了ALS基因SOD1的水平,”穆勒博士说。“该计划的下一步将是在安慰剂对照试验中测试第二代临床候选药物的临床疗效。”
虽然该研究中的第一位患者经历了对治疗载体的炎症反应和相关的局灶性疼痛综合征,但第二位患者使用免疫抑制剂缓解了这一问题。免疫抑制剂只在注射时使用,当传递载体上的病毒衣壳从体内被清除时,免疫抑制剂会钝化人体的免疫系统。
“我们从这次重要的合作中获得的见解帮助我们了解治疗的潜在效果,”贝里博士说。“这项早期工作有助于为更广泛的测试铺平道路,这种令人兴奋的、潜在强大的方法可以针对SOD1突变引起的ALS进行测试。”
肌萎缩性侧索硬化症,也被称为卢伽雷氏病,是一种进行性的运动神经元神经退行性疾病。据估计,美国每年有6000人被诊断出患有这种疾病。随着运动神经元的死亡,会出现进行性瘫痪,然后死于呼吸衰竭。ALS患者的平均生存时间为3到5年。1993年,布朗博士领导的一个研究小组发现了第一个与家族性ALS相关的基因,这是一种被称为超氧化物歧化酶(SOD1)的蛋白质抗氧化剂。只有10%的ALS病例是家族性的,而大约90%的ALS病例在性质上是散发的,这意味着没有可识别的家族风险或家族病史。
SOD1基因的毒性突变,如本出版物中描述的试验目标,占ALS遗传病例的20%。一种潜在的治疗方法是抑制突变体的活性基因从而降低有毒蛋白质的水平。至少在动物模型中,这种方法可以减缓甚至逆转运动神经元的死亡。靶向这些基因的一种方法是使用microRNAs。
MicroRNAs是植物和动物中发现的天然RNA沉默机制的一部分。这些小RNA结合并破坏基因的RNA模板,因此细胞不能将RNA转化为蛋白质。利用这种细胞机制,科学家们相信他们可以有效地“关闭”导致疾病的有毒基因和蛋白质。
超过180种不同的SOD1基因突变与渐冻症有关。穆勒实验室确定了这些不同突变的DNA序列的共性,允许团队使用靶向几乎所有不同SOD1突变的RNA序列进行开发。“否则,每个独特的突变序列都需要自己的药物来抑制,”穆勒说。“这种方法使我们能够使用一种药物针对绝大多数患有SOD1突变的患者。”
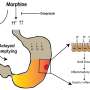
当注入脊髓液时,腺相关病毒能够在整个脊髓长度内传递其抗sod1 microRNA。一旦交付,microRNA减少了脊髓组织中SOD1蛋白的产生。
Brown说:“我们对这些早期结果感到鼓舞和欣慰,因为我们自1993年以来一直在追求抑制SOD1基因。在目前的研究中,似乎有SOD1基因的沉默和临床益处的暗示。同样重要的是,我们学会了如何通过免疫抑制来控制药物的潜在副作用。这有助于我们进行更大规模的研究,从而评估疗效。”
在一篇相关的社论中新英格兰医学杂志奥尔拉·哈迪曼(Orla Hardiman),医学博士,都柏林三一学院神经病学临床教授,三一学院神经科学研究所学术临床医学负责人;荷兰乌得勒支大学医学中心神经学教授兼运动神经元疾病实验神经学主席Leonard H. van den Berg医学博士写道:“这些进展标志着渐冻症治疗的新开始,某些形式的疾病可能会变得可治疗。通过从具有特定基因组特征的亚群开始,研究人员为患有这种毁灭性致命疾病的遗传风险患者提供了新的希望。”