新方法减轻动物模型SCA1症状

研究表明,ATAXIN-1基因的突变导致ATAXIN-1 (ATXN1)蛋白在脑细胞中的积累,是一种罕见的遗传性神经退行性疾病,即脊髓小脑性共济失调1型(SCA1)的根本原因。健康细胞如何维持ATXN1的精确水平仍然是一个谜,但现在贝勒医学院和德克萨斯儿童医院简和丹·邓肯神经学研究所的研究人员领导的一项研究揭示了一种调节ATXN1水平的新机制。
在SCA1动物模型中操纵这一机制可以降低ATXN1水平,并改善病情的一些症状。该研究结果发表在该杂志上基因与发育,提供了开发改善这种无法治愈的疾病的治疗方法的可能性。
SCA1的特征是进行性运动问题,包括丧失协调能力、平衡能力(共济失调)和肌肉无力。患有SCA1的人通常在症状首次出现后存活15到20年,”第一作者Larissa Nitschke说,她是贝勒大学和德克萨斯州儿童医院Huda Zoghbi博士实验室的博士候选人。
“SCA1是成人发病的神经退行性疾病之一,我们知道其遗传原因,在这种情况下是基因ATXN1,”该研究的通讯作者、分子和人类遗传学、儿科和神经科学教授、贝勒大学医学博士拉尔夫·d·费金(Ralph D. Feigin)说。ob体育开户网址“当我们识别出该基因时,我们了解到突变会导致ATXN1蛋白在细胞中停留的时间比正常情况下更长。这对神经元来说是个坏消息,因为过多的ATXN1会导致神经元死亡。”
研究结果表明,降低ATXN1的水平可能会改善症状,因此Nitschke和她的同事们寻找细胞用来控制ATXN1水平的机制。
细胞如何调节ATXN1水平
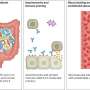
和其他基因ATXN1基因的一部分编码蛋白质本身,其余部分参与调节基因编码的RNA和蛋白质的表达。
Nitschke说:“我们观察了一个被称为5'非翻译区(5' UTR)的调控区域,它对ATXN1基因来说异常长,并发现它可以控制蛋白质,因此它不会积累到有毒水平。”
研究人员对这一区域进行了详细的研究,试图找出可能控制细胞产生ATXN1数量的单个序列或元素。他们发现了几个满足这一功能的元素。
Nitschke和她的同事们专注于一种似乎很重要的调节元素,因为它在许多物种中都是保守的。他们发现这个短片段可以调节ATXN1的水平。
“我们还发现,我们可以减少一种名为miR760的microRNA产生的ATXN1的数量,这种microRNA专门与5'UTR区域的保守小片段结合。MicroRNAs是一种微小的RNA分子,细胞通过与调控区域相互作用来调节特定蛋白质的产生。“这一发现鼓励我们测试miR760是否可以减少SCA1动物模型中ATXN1的数量。”
在动物模型中,减少小脑中的ATXN1可以改善SCA1症状
在SCA1动物模型上测试miR760的效果必须仔细计划。
“ATXN1在大脑中的作用很复杂,”简和丹·邓肯神经学研究所所长、霍华德·休斯医学研究所成员佐格比说。“大脑后部的小脑区域有太多的ATXN1,它涉及平衡和协调,会导致平衡问题。大脑中负责学习和记忆的部分ATXN1过少会增加患阿尔茨海默病的风险。”
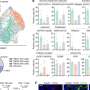
研究人员设计了他们的实验,通过针对小脑区域的基因治疗来降低ATXN1的水平。结果令人鼓舞。提供miR760降低了ATXN1的水平,重要的是,改善了SCA1动物模型中的运动和协调缺陷。
“我们的发现中最令人兴奋的部分是,我们可以在动物模型中减轻SCA1的一些症状,”Nitschke说。“尽管我们只将ATXN1的水平降低了约25%,但小鼠的运动能力却得到了显著改善。这一结果有力地支持了进一步的研究,以探索这种方法治疗人类状况的有效性。”
这些发现不仅强调了ATXN1基因调控区域在SCA1中的重要性,而且还提出了这些DNA元件突变可能导致ATXN1水平升高,进而增加平衡问题风险的可能性。在有平衡问题的人身上识别和分析这些元素的序列可能有助于提供诊断。
更多信息:Larissa Nitschke等人,miR760通过与其5 '非翻译区相互作用调节ATXN1水平,基因与发育(2020)。DOI: 10.1101 / gad.339317.120