精确定位维持人体主生物钟运转的细胞

德克萨斯大学西南分校的科学家开发了一种基因工程小鼠和成像系统,使他们能够可视化小鼠细胞类型的生物钟波动。该方法在杂志的网络版上有描述神经元这项研究让我们对哪些脑细胞在维持人体主生物钟方面很重要有了新的认识。但他们表示,这种方法也将广泛用于回答关于全身细胞日常节律的问题。
“这是推进昼夜节律研究的一个非常重要的技术资源,”研究负责人约瑟夫·高桥博士说,他是德克萨斯大学西南医学中心神经科学系主任,德克萨斯大学西南医学院彼得·奥唐奈脑研究所的成员,也是霍华德·休斯医学研究所(HHMI)的研究员。“你可以将这些鼠标用于许多不同的应用。”
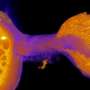
几乎人类和小鼠的每个细胞都有一个内部的生物钟,大约以24小时为周期波动。这些细胞帮助不仅决定了饥饿和睡眠周期,还决定了免疫和新陈代谢等生物功能。生物钟的缺陷与癌症、糖尿病、阿尔茨海默氏症以及睡眠障碍等疾病有关。科学家们早就知道,大脑的一小部分——视交叉上核(SCN)——将来自眼睛的关于环境明暗周期的信息与身体的主时钟整合在一起。反过来,SCN有助于保持体内其他细胞彼此同步。
高桥说:“使SCN成为一种非常特殊的时钟的原因是它既坚固又灵活。”“这是一个非常强大的起搏器,不会失去时间的轨迹,但同时可以调整以适应季节,改变一天的长度,或在时区之间旅行。”
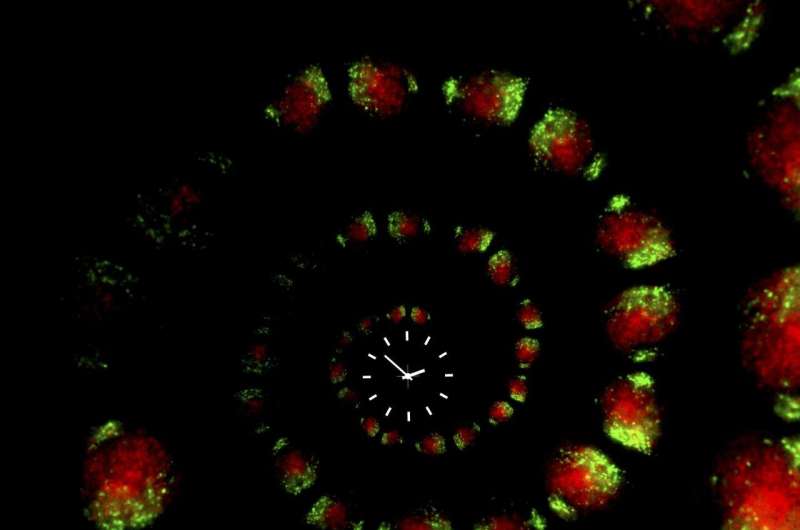
为了研究生物钟在SCN和身体的其他部分,高桥的研究小组之前开发了一种具有生物发光版本per2的小鼠,per2是一种关键的昼夜节律蛋白,其水平在一天中波动。通过观察生物发光水平的增减,研究人员可以看到PER2在白天是如何在动物体内循环的。但这种蛋白质几乎存在于身体的每个部位,有时会使人难以区分混合在同一组织中的不同细胞类型之间的昼夜周期差异。
高桥说:“例如,如果你观察大脑切片,几乎每个细胞都有PER2信号,所以你无法真正区分任何特定的PER2信号来自哪里。”
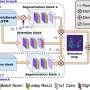
在新的研究中,科学家们通过一种新的生物发光系统克服了这个问题,这种系统只在表达一种名为Cre的特殊基因的细胞中改变颜色——从红色变成绿色。然后,研究人员可以改造小鼠,使Cre在小鼠细胞中不存在,一次只存在于一种细胞类型中。
为了测试这种方法的实用性,高桥和他的同事研究了构成大脑scn -精氨酸抗利尿激素(AVP)和血管活性肠多肽(VIP)细胞的两种细胞。在过去,科学家们假设VIP神经元掌握着保持SCN其余部分同步的关键。
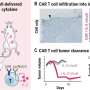
当研究小组观察VIP神经元时——只在这些细胞中表达Cre,因此PER2在VIP细胞中发出绿色的光,而在其他地方发出红色的光——他们发现,从神经元中去除昼夜节律基因对VIP神经元或SCN的其余部分的昼夜节律几乎没有整体影响。“即使VIP神经元不再具有功能时钟,SCN的其余部分表现基本相同,”UTSW研究科学家、该研究的主要作者单永利博士解释说。他说,附近的细胞能够向VIP神经元发出信号,使它们与SCN的其余部分保持同步。
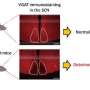
然而,当他们在AVP神经元上重复同样的实验——去除关键的时钟基因——不仅AVP神经元本身表现出节律紊乱,而且整个SCN也停止了正常的24小时同步循环节奏.
“这向我们表明,AVP神经元中的时钟对于整个SCN网络的同步非常重要,”Shan说。“这是一个令人惊讶的结果,有点违反直觉,所以我们希望它能带来更多关于AVP的工作神经元前进。”
高桥说,其他研究昼夜节律的研究人员已经向他的实验室申请了小鼠系,以研究其他细胞的日常周期。他说,这些小鼠可能会让科学家们深入研究单个器官内不同细胞类型之间的昼夜节律差异,或者肿瘤细胞与健康细胞的周期差异。
“在各种复杂或患病的组织中,这可以让你看到哪些细胞有节奏,以及它们与其他细胞类型的节奏有什么相似或不同。”