研究人员发现方法在关节中再生包装
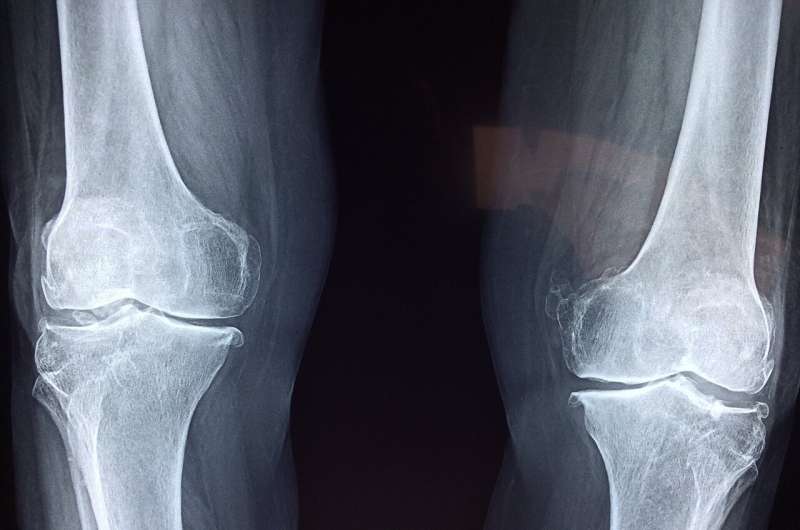
斯坦福大学医学院(Stanford University School of Medicine)的研究人员发现了一种在小鼠和人体组织中再生关节软骨缓冲层的方法。
丧失这种滑爽和减震吸收组织层,称为关节软骨,是许多案件的罪魁祸首关节疼痛以及折磨着5500多万美国人的关节炎。近四分之一的成年美国人患有关节炎,而更多的人通常受关节疼痛和炎症的折磨。
斯坦福大学的研究人员找到了使关节软骨再生的方法:首先对关节组织造成轻微损伤,然后在损伤愈合时使用化学信号来引导骨骼干细胞的生长。这项研究于8月17日发表在该杂志上自然医学。
外科助理教授查尔斯·k·f·陈博士说:“软骨在成年后几乎没有再生潜力,所以一旦它受伤或消失,我们能为患者做的就非常有限。”“找到一种帮助身体再生这种重要组织的方法是非常令人满意的。”
这项工作建立在斯坦福大学之前的研究基础上,该研究分离了骨骼干细胞,这是一种自我更新的细胞,也负责生产骨软骨和一种帮助血细胞生长的特殊细胞骨髓。这项新的研究,就像之前对老鼠和人类骨骼干细胞的发现一样,大多是在陈和外科教授迈克尔·朗格医学博士的实验室里进行的。
关节软骨是一种复杂而特殊的组织,在关节处的骨头之间提供光滑和有弹性的缓冲。当这个软骨受到创伤、疾病或随着年龄的增长而变薄时,骨头就会直接相互摩擦,引起疼痛和炎症,最终导致关节炎。
损坏的软骨可以通过称为微折衷的技术处理,其中微小的孔在接头的表面钻孔。微折衷技术促使身体在关节中产生新的组织,但新组织并不像软骨一样。
“微骨折导致了所谓的纤维软骨,它更像疤痕组织,而不是天然软骨,”Chan说。“它覆盖着骨头,总比什么都没有好,但它没有天然软骨的弹性和弹性,而且退化的速度相对较快。”
最近的研究是通过Surgeon Matthew Murphy,博士的工作,斯坦福大学的斯坦福大学博士的工作。“我从来没有觉得任何人都真的明白了微折悔如何真正锻炼,”墨菲说。“我意识到了解过程的唯一方法是看微碾压后干细胞正在做什么。”墨菲是纸上的牵头作者。陈和朗克是共同高级作者。
很长一段时间,陈说,人们假设在受伤后没有再生成虫,因为组织没有可以激活许多骨骼干细胞。在鼠标模型中工作,该团队记录了微折衷确实活化骨干细胞。然而,留给了自己的设备,这些活化的骨干干细胞在关节中再生纤维纤维。
但是,如果微折衷后的愈合过程可以转向软骨的发展,以及远离纤维纤维,那么怎么办?研究人员知道,随着骨骼的发展,细胞必须先通过软骨阶段进入骨骼前。他们认为,他们可能会鼓励关节中的骨骼干细胞沿着变成骨的道路开始,但停止在软骨阶段的过程。
研究人员使用称为骨形态发生蛋白2(BMP2)的强大分子以在微折衷后引发骨形成,但随后将过程中途停止,分子阻断骨形成的另一种信号分子,称为血管内皮生长因子(VEGF)。
“我们最终的软骨是用相同的电池制成的软骨,与我们通常得到的纤维癣不同的机械性能不同,”陈说。“它还恢复到骨关节炎小鼠的流动性,并显着降低了痛苦。”
为了证明这一原理可能也适用于人类,研究人员转移了人类组织移植到不排斥组织的老鼠身上,并且能够显示出人类骨骼干细胞可以引导骨骼发育,但在软骨阶段停止。
在开始人类临床试验之前,下一个研究阶段是在较大的动物中进行类似的实验。墨菲指出,由于难以使用非常小的鼠标关节,可能对系统的影响可能会产生一些改进,因为它们进入相对更大的关节。
第一个人体临床试验可能是针对手指和脚趾有关节炎的人。Murphy说:“我们可能会从小关节开始,如果可行的话,我们可以向上移动到更大的关节,比如膝盖。”“目前,治疗手指关节炎最常见的手术之一是取出拇指底部的骨头。在这种情况下,我们可能会尝试用这种方法来保存关节,如果它不起作用,我们就把骨头取出来。改进的潜力很大,但缺点是我们可能会回到以前的水平。”
Longaker指出,他们发现的一个优势是,一种潜在疗法的主要成分被FDA批准为安全有效的。“BMP2已经被批准用于帮助骨愈合,VEGF抑制剂已经被用作抗癌疗法,”Longaker说。“这将有助于加快我们开发的任何疗法的批准。”
关节置换手术彻底改变了医生治疗关节炎的方式,而且它非常常见:到80岁时,每10个人中就有一个要做髋关节置换,每20个人中就有一个要做膝盖置换。但这种关节置换具有极强的侵入性,寿命有限,而且只有在关节炎发作、患者忍受了持久的疼痛后才会进行。研究人员表示,他们可以设想将来有一天,人们可以通过在关节软骨严重退化之前恢复其青春,从而避免患上关节炎。
朗格说:“一种想法是遵循‘Jiffy Lube’软骨补充模型。”“你不必等待损伤的累积,你可以定期地使用这个技术来增强你的关节。软骨在你有问题之前。“
进一步探索
deshka s. foster等。阐明驱动腹部粘附形成的基本纤维化过程,自然通信(2020)。DOI:10.1038 / S41467-020-17883-1











用户评论