常染色体显性视神经萎缩是一种无法治愈的视觉丧失障碍
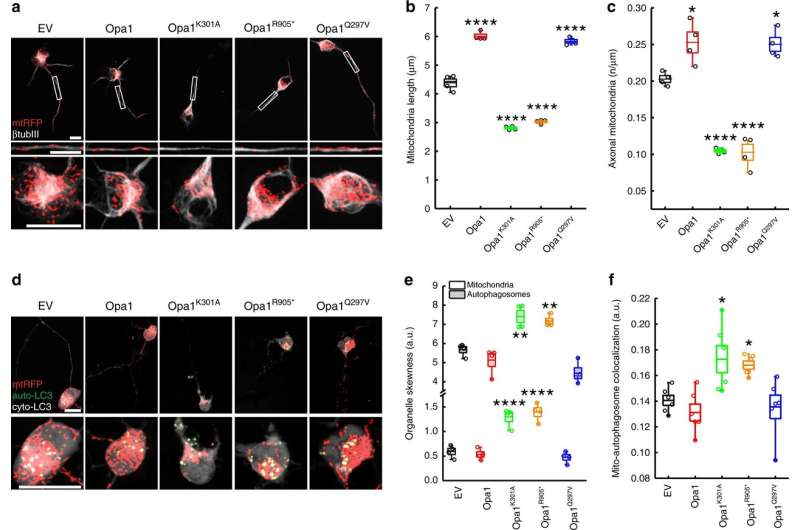
在杂志中自然通讯,研究人员揭示了一种新的分子机制,其潜在的不受控制的线粒体自噬对神经元存活的有害影响,有助于常染色体显性视神经萎缩(ADOA)的发展和进展。
IMBB研究人员Konstantinos Palikaras博士和Nektarios Tavernarakis博士(克里特岛大学医学院教授,FORTH董事会主席)与意大利帕多瓦大学Marta Zaninello博士和Luca Scorrano教授团队合作,证明了过度的神经元自噬会耗尽轴突中的线粒体,并引发线虫和小鼠的神经退行性变。自噬的遗传和药理学抑制恢复神经元过程中的线粒体含量,并逆转ADOA小鼠模型中的视力丧失。
常染色体显性视神经萎缩(ADOA)是最常见的显性遗传性视神经病变,引发视网膜神经节细胞(RGCs)的特异性损失。ADOA临床表现为儿童早期双侧视力丧失。大多数受影响的ADOA病例与OPA1基因突变有关。OPA1是一种调节线粒体动力学的线粒体蛋白。线粒体是所有真核细胞中不可缺少的、能产生能量的细胞器,在基本细胞过程中也起着重要作用。线粒体内稳态的改变严重影响细胞代谢,并严重影响细胞活力。广泛的复杂和高度专业化的分子和细胞途径已经进化以保持线粒体稳态。线粒体自噬是一种选择性的自噬类型,介导功能失调线粒体的消除,是细胞调节线粒体含量以应对代谢应激的主要机制。
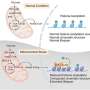
线粒体形态缺陷和线粒体含量降低是ADOA病理生理的主要标志。虽然大量的研究工作集中在开发针对ADOA的新治疗策略上,但目前还没有有效的治疗方法。斯科拉诺教授和塔维尔纳拉基斯教授的研究团队采用了一种多层面的方法,包括小鼠(Mus musculus)和简单的线虫秀丽隐杆线虫(Caenorhabditis elegans),现在证明了这种不受控制的情况mitophagy耗尽视网膜神经节细胞RGCs中的轴突线粒体,导致其进行性变性。重要的是,在线虫和小鼠ADOA模型中,抑制线粒体自噬可以恢复线粒体含量和神经元功能。这些发现确定了线粒体的不受控制的消除是神经退行性变的关键因素,并强调了线粒体的调节作为一种潜在的治疗干预策略。
确定特定的有丝分裂调节剂可能导致有效的治疗干预策略的发展,具有广泛的相关性人类健康和生活质量,解决线粒体相关的疾病,如ADOA。
进一步探索