过敏免疫应答有助于对抗细菌感染
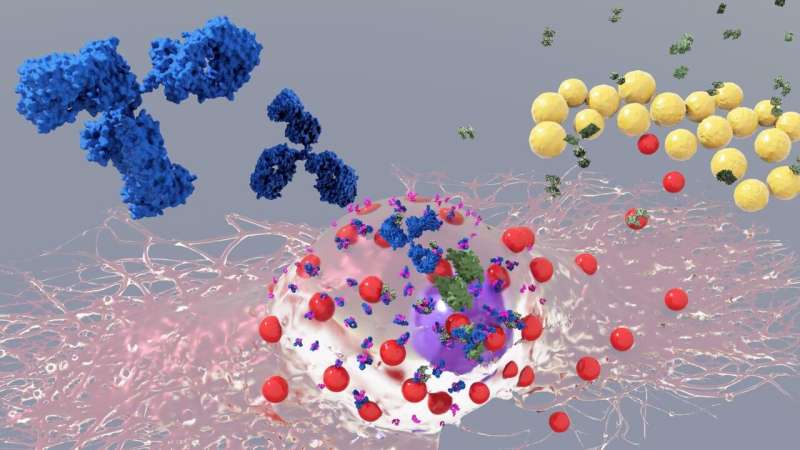
过敏是欧洲最常见的疾病之一,据估计,超过1.5亿欧洲遭受反复化过敏,而2025年这可能增加到整个欧洲人民的一半.1过敏患者最初经历了“致敏的过程”,“这意味着他们的免疫系统发展了一种特定的抗体,所以称为免疫球蛋白E抗体(IgE),其可以识别外部蛋白质,称为过敏原。IGES与表达称为FCεR1的特异性受体的细胞结合并相互作用。体内只有几种细胞类型表达FCεR1受体,并且可能是最重要的是肥大细胞,在整个身体的大多数组织中发现的一种免疫细胞。
当重新暴露于过敏原时,肥大细胞(与其FcεR1受体结合的IgE)通过快速释放不同的介质(例如组胺,蛋白酶或细胞因子),立即反应,导致经典过敏症状。这些症状取决于与过敏原的接触发生的组织,可以从打喷嚏/喘息(呼吸道)到腹泻和腹痛(胃肠道)或瘙痒(皮肤)。全身暴露于过敏原可以同时激活来自不同器官的大量肥大细胞,引起过敏反应,严重和危及生命的过敏反应。
尽管几十年的研究和详细知识对过敏症和肥大细胞的关键作用,但这种“过敏模块”的生理,有益功能仍然没有完全理解。2006年,这项研究高级协作者的Stephen J. Galli及其在斯坦福大学的实验室揭示了肥大细胞对某些蛇和蜜蜂的毒液的先天抗性的重要性。Galli实验室的后续工作表明,“过敏模块”在获得高剂量的毒液中的“过敏模块”的关键作用:这一发现(目前研究的第一个作者的Philipp Starkl重要的是,重要的是第一个明确的实验证据在1991年支持Margie Fumet的“毒素假设”。这一假设提出了对有毒物质的过敏反应的有益功能。
在这次发现之后,维也纳医科大学和CEMM高级博士后研究员菲律宾斯塔尔,与西尔维亚·克纳普,维也纳和CEMM PI教授,以及斯坦福大学医学院教授斯蒂芬J. Galli教授及其同事们试图调查这种现象是否可以在防御其他毒素产生的生物体,特别是致病细菌中相关。作者选择了细菌金黄色葡萄球菌由于其巨大的临床相关性和广泛的毒素,作为病原体模型。该细菌是一种原型抗生素抗性病原体,也与患有哮喘和特应性皮炎等疾病的过敏免疫反应的发育有关。为了他们的研究,他们使用了不同的实验S.金黄色葡萄球菌感染模型与遗传方法和体外肥大细胞模型组合,揭示了IgE效应机制的选定组分的功能。
科学家发现小鼠有一个温和的小鼠S.金黄色葡萄球菌皮肤感染发生针对细菌组分的适应性免疫应答和特定IgES抗体。这种免疫应答在遇到严重的继发性肺或皮肤和软组织感染时,这些小鼠的阻力增加了增加的阻力。然而,缺乏功能性IgE效应器机制或肥大细胞的小鼠无法建立这种保护。这些发现表明,对细菌的“过敏性”免疫反应不是病态的,而是保护性。因此,防御毒素的生产致病细菌可能是过敏模块的重要生物功能。
本研究是菲利普斯特克尔于斯坦福大学的斯蒂芬J. Galli实验室发起的重要合作,以及其他同事,然后在CEMM和维也纳医科大学的Sylvia Knapp实验室继续进行。这种令人兴奋的发现不仅可以推进对免疫系统的一般性理解和最符合的过敏免疫反应,但它也可以解释为什么身体在整个进化过程中保持过敏模块。尽管对过敏性疾病,IGES和桅杆有危险贡献细胞可以施加有益的功能免疫系统可以利用毒素和毒素的细菌保护身体,以保护身体和感染S.金黄色葡萄球菌。
进一步探索












用户评论