新的抗体成熟技术产生高亲和力氨基酶2抗体
癌症研究的研究人员在英国剑桥的抗体联盟联盟实验室开发了一种创新的亲和成熟技术,以产生抑制抑制性,高亲和力抗体(Arg2),该酶意味着包括在内的主要人类疾病癌症。他们的调查结果今天(星期四)在MAB上发表,之后发表了这种方法美国国家科学院院刊.
Arg2靶向并摧毁L-精氨酸,对免疫细胞至关重要的氨基酸,以对抗癌症等疾病以及感染。尽管arg2是控制身体中的精氨酸水平所必需的,但它在各种类型的癌症中过表达,包括胰腺导管腺癌,肠癌和急性髓性白血病。
在这些癌症中,过量的ARG2会大幅降低肿瘤周围的l -精氨酸水平,阻碍需要它的免疫细胞发挥功能,创造一个免疫抑制的局部环境,使肿瘤不受抑制地生长,对免疫系统“隐藏”。因此,ARG2是抑制治疗性抗体的一个有吸引力的靶点,可以帮助恢复针对癌细胞的免疫功能。
Maria Groves博士和她的团队在Cambridge的癌症研究英国 - Astrazeneca抗体联盟,与Cerundolo的后期和他在牛津大学的队伍合作,并在莱斯特大学的Mark Carr教授的结构生物学集团发布了一个对arg2的高度有前途的潜在治疗抗体。称为C0021158的铅抗体是研究人员的创新抗体亲和力成熟方法的第一个产物上个月在PNA中报道的方法,并且具有完全补充所需的性质,包括高亲和力结合和完全抑制Arg2活性的抑制。
传统的亲和力成熟方法专注于探索抗体的少数特定区域的序列多样性,限制了在候选治疗中获得的改进——特别是对成熟具有挑战性的抗体。用于开发C0021158的创新方法使研究人员能够识别具有不可预测的氨基酸序列变化组合的抗体,这种氨基酸序列变化产生了显著提高的亲和力和对ARG2的抑制效力。开创性的抗arg2治疗性抗体的工作戏剧性地说明了新的无偏方法的优势。
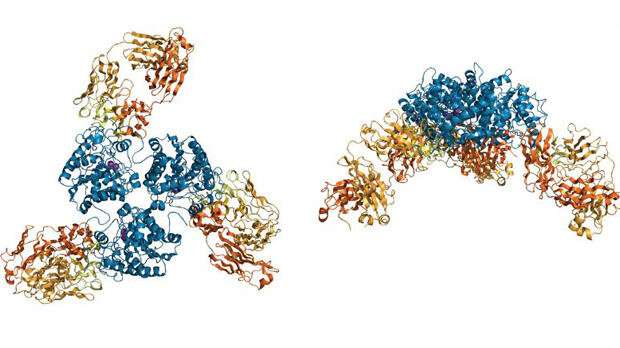
C0021158的表征突出了研究人员在产生治疗候选方面的响亮的成功,这证明了对ARG2活性的完全和高度有效的抑制;在实验室测定中,抗体恢复了增殖免疫细胞通过Arg2驱动的精氨酸缺乏抑制了这一点。在莱斯特大学进行的蛋白质晶体学,提供了抗体介导的抑制机制的关键结构和分子见解,揭示了与亲和成熟产生的抗体相互作用的巨大变化。抑制性抗体结合诱导arg2结构的显着变化,导致酶的活性位点的构象变化,其防止arg2活性和其精氨酸靶标的生产结合。
研究人员预计这些论文中描述的技术将推出通过无偏见的亲和力成熟的新一代高亲和力和高效治疗剂的发现。在候选抗体难以成熟的情况下,这将特别重要,并且将在癌症和超越中具有治疗应用。
来自英国癌症研究所-阿斯利康抗体联盟实验室的研究作者Maria Groves博士说:“将一种新的治疗性抗体带到诊所需要大量的时间和资源,所以我们需要他们尽可能做到最好。”这第一次成功让我有信心,我们公正的图书馆将产生更强大,更有效的抗体,并支持未来新型肿瘤治疗的交付。“
仍然有很长的路要走了新的arg2抗体,研究人员现在希望与公司合作,帮助发展抗体,并进入肿瘤学和非肿瘤学适应症的临床。对于肿瘤学,他们认为,当与化疗或免疫疗法组合使用时,它可能有助于靶向免疫系统的肿瘤。
项目的结构生物学领导者,教授Mark Carr,来自莱斯特大学的结构和化学生物学研究所说:“Arg2治疗抗体项目的突出成功是药物发现中获得的实质益处的示例通过利用制药行业,生物医学慈善和大学部门提供的互补科学专业知识和知识。该项目从Cruk-Astazeneca抗体联盟和我的结构生物学群体的成功结果指出期待进一步成功的合作。“
来自牛津大学的MRC人类免疫学单位的Andreas Hadjinicolaou说:“我们与抗体联盟实验室的合作改变了一个在牛津大学出生的想法,以极其高效和科学的强大的方式成功。实验室申请创新抗体技术阻止arg2酶的免疫逃避效应癌症.这种重点合作产生了特殊的结果和实验室的产出无疑是为了为未来提供新的肿瘤学治疗。这是这项努力的一部分,这是一种愉快和荣幸。“
进一步探索
Decice T. Y. Chan等人。通过无偏见的亲和力成熟使得氨基酶2抑制抗体的广泛序列和结构演变,美国国家科学院院刊(2020).DOI: 10.1073 / pnas.1919565117
Tomasz M. Grzywa等。肿瘤细胞衍生的癌症免疫反应中的氨基酶,免疫学前沿(2020).DOI: 10.3389 / fimmu.2020.00938














用户评论