脑细胞死亡在als,痴呆症与核中的关键生化运输结构丢失
长期以来,研究人员旨在准确地解释与肌萎缩侧面硬化(ALS)和额定仪性痴呆症相关的最常见的遗传突变引起神经细胞的死亡。现在,Johns Hopkins医学研究人员报告了新的证据表明,突变慢慢地破坏了细胞控制中心的蛋白质,酶和其他材料的重要传输系统,这是最终杀死脑和脊髓内神经元的过程。
研究人员说他们的发现,于7月15日在线描述神经元,证实途径作为为ALS和第二种最常见的痴呆症开发新治疗的途径。影响估计的30,000名美国人的ALS是一种浪费的疾病,其中神经元涉及控制肌肉和运动,死亡。患病的人慢慢失去移动,吞咽和呼吸的能力。终身痴呆症,估计折磨高达60,000名美国人,标志着阿尔茨海默病的症状,抢劫记忆,学习能力,人格和情绪稳定。任何疾病都没有建立的治疗方法。遗传突变C9ORF72呼叫C9短暂,在约40-50%的人群中发现,遗传性ALS的约40-50%,约有12%的人患有遗传态颞态痴呆。
"The way we think this common mutation works is like a first scratch on a new car that, if let go over time, rusts the whole car until it won't work," says Jeffrey Rothstein, M.D., Ph.D., director of the Brain Science Institute and the Robert Packard Center for ALS Research and professor of neurology at the Johns Hopkins University School of Medicine.
从Rothstein的实验室的过去的工作证明,许多神经变性疾病(包括ALS)中的共同机制是破坏酶,RNA和蛋白质的运输,并从神经细胞核中脱离含有遗传密码的对照中心。当这种运输被堵塞时,神经元随着时间的推移而死亡。这些小分子在核中移动到数千孔,被称为核心孔隙,各自由30种不同种类的蛋白质构建块组成,称为核锁骨。
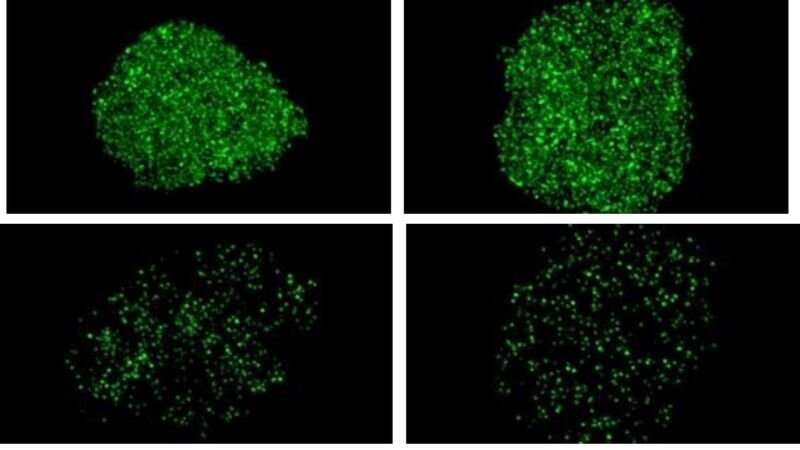
在进一步了解该过程中,新的研究由Alyssa Coyne,博士学位领导,罗斯坦实验室的博士后研究员,为30个核奥蛋白蛋白的23个添加了微小的化学标签,使他们能够看到核心毛孔使用超分辨率显微镜。
然后他们比较了毛孔健康神经元的交通与患有C9 ALS /痴呆引起的突变的人的神经元。在C9神经元中,研究人员表示,它们始终如一地看到了八个不同核磁素的水平,这表明孔隙缺失这些核话“位和碎片”,导致后一种细胞中的运输途径破坏。
使用细胞工程的标准工具,研究人员加入了八个核偶姻基因中的每一个,以产生更高水平的核致核苷蛋白,从而“重建”在C9细胞中的孔与ALS /痴呆引起的突变。他们发现,添加了编码POM121核毒素的基因,也是所有七个核孔的水平,并恢复细胞材料的运输进出核。
“通常,当你将C9神经元进行压力时,他们会死。但是,当我们加回缺少的POM121时,孔子”重建“,C9神经元在压力时没有死亡,”Rothstein说。根据研究人员,POM121是一种结构蛋白质,其将核孔的内环和外圈连接并将它们锚固在核膜中。
C9 Als / Demendia突变以何种方式导致这种伤害核孔?C9 Als /痴呆突变是由DNA字母GGGGCC的重复序列引起的。该DNA序列转化为使RNA“重复”的RNA,其异常过程,其对几种不同蛋白质的指令发出了几种不同的蛋白质序列。研究人员没有确定RNA重复或蛋白质是否重复,导致疾病的后期进展,Rothstein笔记。
为了了解具有C9 ALS /痴呆引起的突变的神经元中RNA或蛋白质重复,导致核毛孔分开,研究人员检查了一种具有除去整个C9ORF72 DNA序列的神经元。如果没有这种DNA序列,神经元不能使RNA或蛋白质自身重复。然后它们以各种组合的蛋白质重复添加,虽然这些蛋白质重复在细胞中,但它们发现蛋白质重复不会影响核OOPOORIN蛋白质水平。另外,它们在这些神经元中添加了RNA重复,而没有C9 DNA,发现相同的减少的核常蛋白蛋白神经元来自Als / Dementia患者C9突变。
“这一发现证实,靶向RNA的药物在C9突变的人中重复的药物可能是治疗ALS或患者的方法圆颞痴呆症通过干扰“生锈”过程,“杜诺斯说。”有希望的是,临床试验中有几种药物,通过与它们结合并将它们作为ALS的治疗来靶向RNA重复。“














用户评论