阻止白血病复发的新方法在小鼠身上显示出了希望
研究人员已经发现了战胜慢性骨髓性白血病的第二种途径。即使面对现有药物的耐药性,慢性骨髓性白血病也倾向于影响老年人。
这项新发现发表于9月17日自然通信。
几乎所有患有慢性粒细胞性白血病CML有一个错误的致癌基因,或称为BCR-ABL1的“致癌基因”。BCR-ABL1可以转化为常规干细胞(一种独特的细胞类型,可以转化为其他类型的细胞然后在骨髓中再现生命期间的那些细胞中的CML干细胞,其产生畸形的血细胞。而不是CML干细胞死亡,当应该调度这样做时,癌基因会导致它继续产生更多这些故障的血细胞。
治疗进展以来,千年之际在对抗这种癌基因患者的疾病方面非常成功。毒品叫酪氨酸激酶抑制剂(TKI)已经完全改变了白血病患者的预后,并且减少了其他癌症治疗的副作用。在大多数情况下,癌症会得到缓解,患者在确诊后还能活很多年。
BCR-ABL1指导一种异常类型的酪氨酸激酶的产生,这种酶通过被称为信号转导的级联化学反应“激活”许多类型的蛋白质——实际上是通过化学通信。由有缺陷的酶引起的交流错误促进了白血病细胞的生长。通过阻断CML干细胞内部的这种通讯,TKI信号转导疗法抑制了CML干细胞的生长,停止了畸形血细胞的产生。
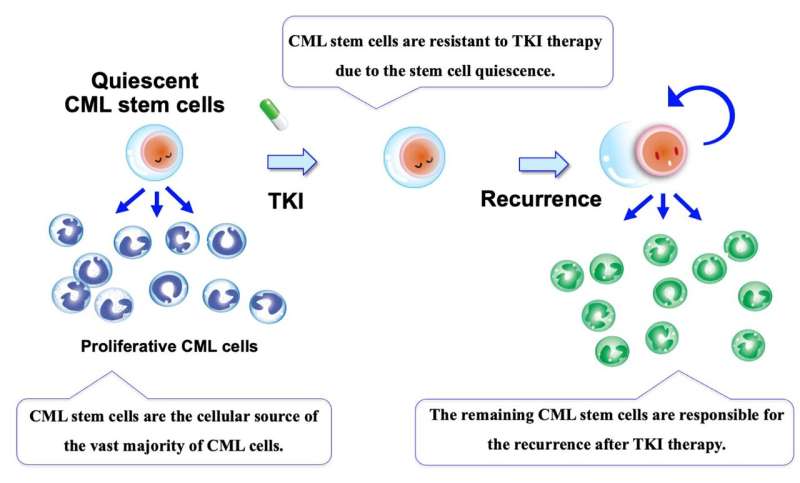
然而,TKIs只能控制疾病;他们不能治愈它。患者可能会产生耐药性,因为虽然TKIs对增殖成熟CML细胞有效,但对静止的CML干细胞,它们在诱导细胞死亡方面效果较差。
静止是细胞生命周期中的一个“闲置”阶段,在这个阶段中,细胞基本上只是休息和悬挂一段时间,以期待重新激活,既不复制也不死亡。
“如果CML干细胞处于静止阶段,否则远离TKI治疗,所以生存可能导致复发,“说Kazuhito纳卡,论文作者和干细胞生物学部门的副教授广岛大学研究所的辐射生物学和医学。
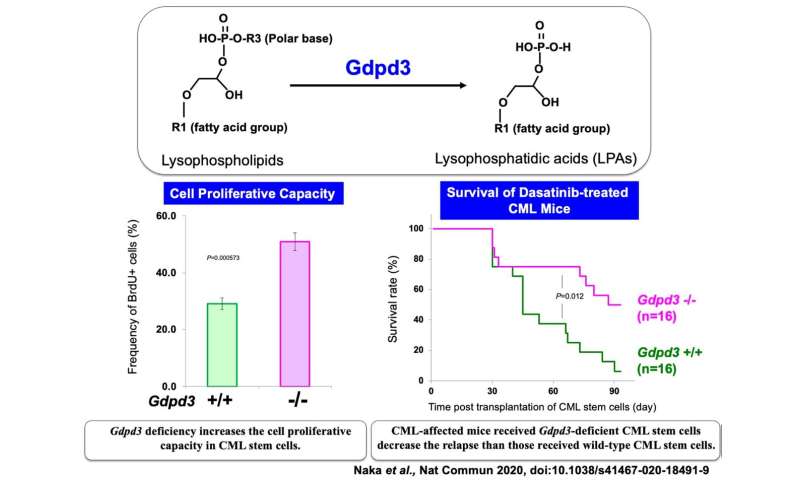
但研究人员在小鼠模型中发现,如果它们破坏GDPD3-A不同的非癌基因基因 - 那么CML干细胞的自我更新能力急剧下降。GDPD3指示特定类型的脂质的酶的生产,该脂质似乎在调节CML干细胞以癌基因的时装时发挥关键作用。
换句话说,Gdpd3基因参与这种脂质的生产,在很大程度上负责维持CML干细胞。研究人员打破了沉默。
至关重要的是,当研究人员破坏编码这些脂质的Gdpd3基因时,即使BCR-ABL1致癌基因没有被破坏,小鼠的白血病复发也显著减少。
Naka博士说:“除了必须与BCR-ABL1致癌基因搏斗之外,这可能提供了另一种途径来抑制这些白血病——也许还有其他癌症。”
虽然研究人员对这种特殊的脂质引起CML的复发发现了一种新的生物学上具有重要作用,但它们仍然没有完全理解这种情况的精确方式。研究人员现在想调查所涉及的机制以及这种脂质是否也在癌症干细胞的静态中起作用,导致实体肿瘤,不仅在白血病中,因此也在这些癌症的复发和生长中。
进一步探索













用户评论